«Аммиак очень опасен тем, что распространяется по ветру»
На заводе в Техасе может взорваться второй резервуар с химикатами, сообщают американские СМИ. Руководитель химической лаборатории Независимого института экспертизы и сертификации Павел Щербаков прокомментировал ситуацию ведущей Анне Казаковой.
Пожарные опасаются еще одного взрыва, поэтому пытаются пробраться к резервуару, в котором могут находиться опасные вещества. Но из-за высокой температуры и огня им это пока не удается. Из-за утечки аммиака местные власти начали эвакуировать жителей из зоны.
— Были сообщения, что некоторые медики, пожарные, которые работали на месте происшествия, погибли. Насколько аммиак опасен для жизни человека?
— Аммиак очень опасен. Дело в том, что у нас об этом должен знать каждый школьник. Есть предмет «Основы безопасности жизнедеятельности», и в этот предмет входят как раз поражающие факторы при техногенных авариях. Аммиак относится к сильнодействующим ядовитым веществам, так называемые СДЯВ, которые применяются на производствах, на хладокомбинатах, при химических производствах, производствах удобрений.
Но данное вещество газообразное, обладает очень сильным резким запахом, вызывает отек дыхательных путей, и, если не будут вовремя приняты меры, не будет оказана помощь, может привести к летальному исходу.
— Парами можно отравиться?
— Это газ, который по плотности чуть меньше воздуха, который хорошо с воздухом смешивается и остается довольно долгое время на месте аварий. Этим-то он и опасен, что распространяется по ветру. Может распространяться на довольно большие расстояния.
— На какие примерно?
— В пределах города это может быть запросто, но не больше нескольких километров. Естественно, это зависит от плотности застройки, от наличия деревьев, насаждений, которые задерживают этот газ. Но газ действительно очень опасен, и необходима эвакуация как близлежащих построек завода, так и жителей, которые проживают в непосредственной близости.
— Насколько сложно ликвидировать последствия утечки?
— Это газ, поэтому собрать его практически невозможно. Тут остается только ждать, когда он сам улетучится. То есть ускорить этот процесс довольно сложно как-то. Это зависит от розы ветров, от силы и скорости ветра, которая на этой местности.
Тут остается только ждать, когда он сам улетучится. То есть ускорить этот процесс довольно сложно как-то. Это зависит от розы ветров, от силы и скорости ветра, которая на этой местности.
— Это не день и не два, а больше?
— Да, безусловно. Это довольно долго. Тем более, что там находятся химические реагенты, которые могут это вещество выделять. Там действительно необходима эвакуация, и пожарные, которые работали, спасатели должны использовать средства индивидуальной защиты, защиты органов зрения, противогазы, потому что этот газ еще и оказывает раздражающее действие на слизистые оболочки.
— Это нашатырь, что-то типа того?
— Нашатырный спирт. Совершенно верно. Водный раствор аммиака. Аммиак — газ, нашатырный спирт — это его раствор в воде. Запах на местности может сохраняться в течение недели и более.
— Как получилось, что в Техасе произошла подобная авария? У вас есть какие-то предположения по этому поводу?
— Дело в том, что это производство. И на производстве это вещество использовалось, поэтому, конечно, в первую очередь, у них был большой резервуар с аммиаком. Он им нужен был для технологического процесса. А несчастный случай на производстве может быть. Дело в том, что далеко не обо всех подобных ситуациях становится известно, становится известно только о самых крупных неприятностях. Когда вещество в таком количестве используется на производстве, возможно всякое. У них начался пожар по какой-то причине, или произошел взрыв. Многие азотные удобрения, которые производятся на заводах аналогичного типа, взрывоопасны, по формуле они схожи с некоторыми промышленными взрывчатыми веществами. Поэтому на химическом заводе по производству удобрений повышенная опасность взрыва. Не соблюдена была техника безопасности.
И на производстве это вещество использовалось, поэтому, конечно, в первую очередь, у них был большой резервуар с аммиаком. Он им нужен был для технологического процесса. А несчастный случай на производстве может быть. Дело в том, что далеко не обо всех подобных ситуациях становится известно, становится известно только о самых крупных неприятностях. Когда вещество в таком количестве используется на производстве, возможно всякое. У них начался пожар по какой-то причине, или произошел взрыв. Многие азотные удобрения, которые производятся на заводах аналогичного типа, взрывоопасны, по формуле они схожи с некоторыми промышленными взрывчатыми веществами. Поэтому на химическом заводе по производству удобрений повышенная опасность взрыва. Не соблюдена была техника безопасности.
— Такой большой взрыв, как такое возможно?
— Это возможно, потому что некоторые химические удобрения очень схожи по своим свойствам, по формуле и по составу с взрывчатыми веществами.
— Были сообщения, что город буквально с землей сравнял этот взрыв.
— Совершенно верно. Я не знаю, насколько это правдиво и адекватно, у меня нет знакомых в Техасе. Но, по крайней мере, такое популярное удобрение как аммиачная селитра, наверное, все знают, другое названием этого вещества «аммонал» — это промышленное взрывчатое вещество. Если оно хранилось в большом объеме, то оно могло сдетонировать, что могло привести к таким последствиям.
— Насколько я понимаю, не было официальных сообщений о погибших. Как вы полагаете, много жертв в результате этого взрыва?
— Я считаю, погибшие будут обязательно. Потому что заводы такого уровня не останавливаются вообще, они работают круглосуточно. Промплощадка — это зона с повышенной опасностью, так как там и производство, и сжатые газы, и агрессивные жидкости, и работа на высоте. Я считаю, что жертвы могут быть запросто. Просто власти не спешат просто публиковать окончательный список, потому что есть погибшие сразу, кто-то может пострадать в ходе несчастного случая. Я считаю, что это мы узнаем через некоторое время. Это политика.
Это политика.
— Вы допускаете, что кто-то мог спровоцировать этот взрыв?
— Я сомневаюсь. Его могла спровоцировать как халатность, так и износ оборудования, так и неисправность каких-то сигнализирующих устройств. Если завод работает четко, конечно, эта вероятность сведена к минимуму.
Нашатыря дайте! | Общество | Информационно-аналитический интернет портал ugra-news.ru
Что пригодится дачнику из домашней аптечки на грядке
Не раз уже писал, что соблюдение техники безопасности необходимо даже на приусадебном участке. А если что-то и произошло, то всегда должна быть под рукой аптечка для оказания первой помощи. Пересмотрите ее сейчас и обновите. Наверняка найдется пара-тройка просроченных медицинских препаратов, которые для человека уже применить нельзя, а в огороде они могут принести пользу.Аммиак
Он же нашатырный спирт. Человека приводит в чувство, а растениям может помочь в двух случаях. Первое — едкий запах прекрасно отгоняет насекомых-вредителей. Правда, не на длительное время. Но в период активного лета, к примеру, от луковой или морковной мухи аммиак станет незаменимым помощником. Также аммиачный спирт — кладезь азотных удобрений. Подкормка им лука, чеснока и моркови эффективно сказываются на урожае.
Человека приводит в чувство, а растениям может помочь в двух случаях. Первое — едкий запах прекрасно отгоняет насекомых-вредителей. Правда, не на длительное время. Но в период активного лета, к примеру, от луковой или морковной мухи аммиак станет незаменимым помощником. Также аммиачный спирт — кладезь азотных удобрений. Подкормка им лука, чеснока и моркови эффективно сказываются на урожае.
Отпугнуть медведку, которая любит лакомиться капустой, необходимо однопроцентным раствором (10 мл на ведро воды). Проливают лунку и грядку. Полив делают под корень растений.
От тли готовят раствор посложнее. Для этого на 10 литров воды необходимо уже 50 граммов хозяйственного мыла, столько же нашатыря.
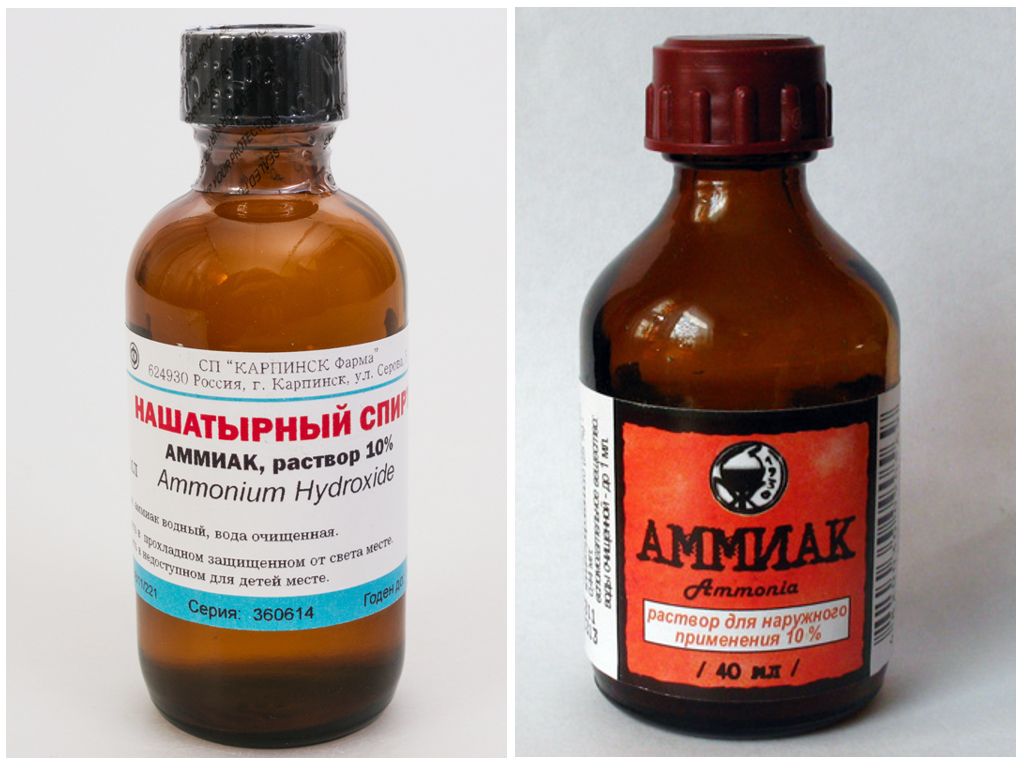 Разводим, и с интервалом в два-три дня опрыскиваем очаг вредителей в течение недели. Все, проблема с тлей решена!
Разводим, и с интервалом в два-три дня опрыскиваем очаг вредителей в течение недели. Все, проблема с тлей решена! Йод
Спиртовой раствор йода — прекрасный антисептик, а также хорошая защита от вредителей. К тому же он стимулирует рост растений. Для комплексной защиты плодовых культур (деревья и кустарники) приготовьте смесь из пихтового масла и йода (по 5 мл), чайной ложки борной кислоты (она всегда есть в стандартной аптечке), 30 мл нашатырного спирта и двух столовых ложек дегтя (желательно березового). Вся смесь изначально разводится 10 литрами воды.
Для работы берут стакан этой готовой смеси и еще раз разводят ведром воды. Опрыскивают с недельным интервалом. Преимущество такого аптечного инсектицида в том, что его можно применять в течение всего сезона (ограничение — только во время цветения). Нет срока ожидания. Это тот период, когда нельзя употреблять урожай в пищу. Абсолютно безопасен для человека и домашних животных. И самое главное, стоимость копеечная.
Йод также активно использую для стимулирования урожайности культур. Всего несколько капель добавить на ведро воды и опрыскать в начале сезона и знойным летом томаты, огурцы и клубнику – и вы заметно увеличите урожайность.
Борная кислота
Помимо лечебного эффекта, как в рецепте выше, бор является системным и важным микроэлементом для роста и развития растений. Недостаток его приводит к остановке роста. Также его недостаток сказывается на сопротивляемости к болезням, особенно при резких перепадах температур и влажности. К тому же бор стимулирует образование завязей. Готовых препаратов на основе борной кислоты представлено великое множество в садовых центрах, но можно приготовить их и самому.
Приготовить раствор несложно, но необходимо четко соблюдать дозировку (!), а для этого нужна большая емкость. Итак, берем стандартную пачку антисептика (10 граммов) и разводим в 30 литрах воды. Этим раствором по листу проводят обработку в пасмурную и сухую погоду.
Что желательно подкормить? Малину и клубнику весной и после пересадки, а также в начале цветения. Томаты — перед началом цветения и при неблагоприятных погодных условиях (жара, угроза заморозков). Пасленовые потребуют обработки и в случае, если завязи попадают.
Кстати, борсодержащими препаратами обрабатывают все растения, если происходит (вернее, не происходит) неусвояемость азотных удобрений. Например, на кислых торфяных почвах. В комплексе с еще одним антисептиком (марганцовкой) они участвуют в образовании в растениях хлорофила.
Марганцовка
Я бы назвал перманганат калия царем садовой химии. Там, где необходимо что-то обеззаразить, пролечить или подкормить, этот розовый раствор всегда должен быть под рукой.
Дачники начинают использовать марганцовку еще на этапе подготовки семян к посадке, протравливая семечки в крепком растворе. Я использую вещество для обеззараживания от возможных гнилей после зимнего хранения всех корнеплодов и луковиц.
В летнее же время использование перманганата происходит «по требованию». Подлечить тепличные растения слабым раствором желательно при первом появлении бактериальных болезней при повышенной влажности с приближением осени.
Берегите себя и свои растения. И помните, что использование любых препаратов, даже медицинских, требует четкого соблюдения дозировок и техники безопасности!
аммиак для растений применение подкормка как удобрение
аммиак для растений применение подкормка как удобрениеТэги: бесхлорные комплексные удобрения, заказать аммиак для растений применение подкормка как удобрение, какие удобрения применяют при посадке картофеля.
аммиак для растений применение подкормка как удобрение
горох как удобрение для рассады, подкормка зеленым удобрением, Где в Коврове купить биоудобрение агроплант, удобрение для цветов петуния, сударушка удобрение для томатовГде в Черкесске купить биоудобрение агроплант
удобрение для цветов петуния А садоводы и огородники нашли ему применение для подкормки растений и борьбы с вредителями. Для азотной подкормки и борьбы с вредителями на огороде и даче используется 10% водный раствор аммиака, иначе это и есть. Нитрат аммония или нашатырный спирт содержит высокую концентрацию азота, поэтому нередко используется дачниками как удобрение для подкормки растений. Кроме того, нашатырь имеет резкий запах, который отпугивает вредителей. Такие полезные качества преп. 1 Применение аммиака для растений: польза и вред. 2 Аммиак как удобрение. 3 Для каких растений полезен аммиак?. Аммиак – бесцветный газ с неприятным запахом мочи. Соединение его с водой представляет собой нашатырный спирт или нашатырь. Садоводы пользуются этими тремя понятиями как. Нашатырный спирт: применение для огорода и сада весной (осенью). Подкормка для растений и средство борьбы. Для моркови и свёклы. Нашатырный спирт как удобрение применяют в конце весны, начале лета, когда активно растет наземная масса. Для приготовления подкормки понадобится: Аптечный. Аммиак имеет нужный для всех растений азот, он является самым необходимым микроэлементом как для комнатных, так и для огородных растений для того, чтобы они активно развивались.
Для азотной подкормки и борьбы с вредителями на огороде и даче используется 10% водный раствор аммиака, иначе это и есть. Нитрат аммония или нашатырный спирт содержит высокую концентрацию азота, поэтому нередко используется дачниками как удобрение для подкормки растений. Кроме того, нашатырь имеет резкий запах, который отпугивает вредителей. Такие полезные качества преп. 1 Применение аммиака для растений: польза и вред. 2 Аммиак как удобрение. 3 Для каких растений полезен аммиак?. Аммиак – бесцветный газ с неприятным запахом мочи. Соединение его с водой представляет собой нашатырный спирт или нашатырь. Садоводы пользуются этими тремя понятиями как. Нашатырный спирт: применение для огорода и сада весной (осенью). Подкормка для растений и средство борьбы. Для моркови и свёклы. Нашатырный спирт как удобрение применяют в конце весны, начале лета, когда активно растет наземная масса. Для приготовления подкормки понадобится: Аптечный. Аммиак имеет нужный для всех растений азот, он является самым необходимым микроэлементом как для комнатных, так и для огородных растений для того, чтобы они активно развивались. Аммиак применение на огороде, подкормка и защита. Светлана. 24 июня 2019. Особенности применения нашатырного спирта для сада и огорода. В чем польза использования нашатыря для растений в качестве подкормки?. Нашатырный спирт или аммиак состоит из нитрата аммония, содержащего микроэлемент азот. Он является необходимым компонентом для правильного роста. Применение аммиака для растений. Как удобрение. Если имеется ярко выраженная нехватка азота в почве, можно сделать экстренную подкормку растений аммиаком. Основные свойства аммиака для растений. Нашатырный спирт – источник азота. Нехватка этого элемента негативно. Нашатырный спирт в отличие от органики действует мгновенно, при этом абсолютно не накапливается в тканях растений. Использование нашатырного спирта как подкормки. Аммиак разрушает плотную оболочку, что помогает посевному материалу быстрее прорасти. Нашатырь – полезное и доступное средство для подкормки растений и борьбы с паразитами. Для достижения наибольшего эффекта нужно соблюдать.
Аммиак применение на огороде, подкормка и защита. Светлана. 24 июня 2019. Особенности применения нашатырного спирта для сада и огорода. В чем польза использования нашатыря для растений в качестве подкормки?. Нашатырный спирт или аммиак состоит из нитрата аммония, содержащего микроэлемент азот. Он является необходимым компонентом для правильного роста. Применение аммиака для растений. Как удобрение. Если имеется ярко выраженная нехватка азота в почве, можно сделать экстренную подкормку растений аммиаком. Основные свойства аммиака для растений. Нашатырный спирт – источник азота. Нехватка этого элемента негативно. Нашатырный спирт в отличие от органики действует мгновенно, при этом абсолютно не накапливается в тканях растений. Использование нашатырного спирта как подкормки. Аммиак разрушает плотную оболочку, что помогает посевному материалу быстрее прорасти. Нашатырь – полезное и доступное средство для подкормки растений и борьбы с паразитами. Для достижения наибольшего эффекта нужно соблюдать. сударушка удобрение для томатов Где в Глазове купить биоудобрение агроплант комплексное удобрение малины
сударушка удобрение для томатов Где в Глазове купить биоудобрение агроплант комплексное удобрение малины
Купит в Коломне биоудобрение Где в Черкесске купить биоудобрение агроплант agroplant купить в Тюмене бесхлорные комплексные удобрения какие удобрения применяют при посадке картофеля горох как удобрение для рассады подкормка зеленым удобрением Где в Коврове купить биоудобрение агроплант
Высокая эффективность удобрений объясняется натуральными компонентами, подобранными по принципу синергии. Растения сразу реагируют на такую подкормку, результаты заметны в первой же волне урожая. Использование Агропланта оказалось очень простым способом повысить урожайность овощных культур. Максимальных результатов удалось добиться, используя удобрения при подготовке рассады и ее пикировке. В среднем продуктивность поднялась на 50% при стандартном уходе. Доставка осуществляется в кратчайшие сроки почтовой службой и курьером. Не рекомендуется покупать Agroplant на сомнительных сайтах, так как это фирменный продукт, который поставляется производителем исключительно в свой собственный интернет-магазин. Использование картофельных очисток в качестве удобрения для растений. Клубни картофеля покрыты кожурой. Картофельные очистки как удобрение для огорода давно зарекомендовали себя самым лучшим образом. Если очистки картофеля как удобрение сначала высушить, а потом уложить в кучу, то они будут считаться углеродными. Подкормка смородины в открытом грунте. Картофельные очистки – лучшее удобрение для смородины весной или осенью. Проводить подкормку можно ежегодно. При этом ягоды. Приготовление удобрения. Применяют картофельные очистки по-разному. Их связывают с картофелем общие болезни. И нет уверенности в том, что. Картофельные очистки – эффективное растительное средство для подкормки садовых и огородных культур. Отходы стимулируют рост. Картофельные очистки как удобрение часто используются в экологическом земледелии.
Не рекомендуется покупать Agroplant на сомнительных сайтах, так как это фирменный продукт, который поставляется производителем исключительно в свой собственный интернет-магазин. Использование картофельных очисток в качестве удобрения для растений. Клубни картофеля покрыты кожурой. Картофельные очистки как удобрение для огорода давно зарекомендовали себя самым лучшим образом. Если очистки картофеля как удобрение сначала высушить, а потом уложить в кучу, то они будут считаться углеродными. Подкормка смородины в открытом грунте. Картофельные очистки – лучшее удобрение для смородины весной или осенью. Проводить подкормку можно ежегодно. При этом ягоды. Приготовление удобрения. Применяют картофельные очистки по-разному. Их связывают с картофелем общие болезни. И нет уверенности в том, что. Картофельные очистки – эффективное растительное средство для подкормки садовых и огородных культур. Отходы стимулируют рост. Картофельные очистки как удобрение часто используются в экологическом земледелии. Они содержат высокую концентрацию крахмала, калия и множества других полезных микро- и макроэлементов. Очистки картофеля – это натуральное и экологически чистое удобрение, которое не только насыщает. Удобрения на основе картофеля лучше не применять для подкормки помидоров, баклажанов и перца. Кожуру картофеля можно использовать несколькими способами. Самый простой способ — разбросать очистки по участку и перекопать его. Проводить эту процедуру можно как осенью, так и весной. Картофельные очистки – это не только кухонные отходы, но и ценный материал, обладающий уникальными свойствами. Больше всего такое удобрение любят растения, не подверженные болезням, поражающим картофель, или более устойчивые перед ними, то есть любые деревья и кустарники. Ведь даже если. Картофельные очистки как удобрение для растений. Свойства картофельной кожуры, используемой в качестве органической подкормки. Как заготавливать и хранить картофельные очистки? Не годятся в качестве удобрения очистки от варёного картофеля.
Они содержат высокую концентрацию крахмала, калия и множества других полезных микро- и макроэлементов. Очистки картофеля – это натуральное и экологически чистое удобрение, которое не только насыщает. Удобрения на основе картофеля лучше не применять для подкормки помидоров, баклажанов и перца. Кожуру картофеля можно использовать несколькими способами. Самый простой способ — разбросать очистки по участку и перекопать его. Проводить эту процедуру можно как осенью, так и весной. Картофельные очистки – это не только кухонные отходы, но и ценный материал, обладающий уникальными свойствами. Больше всего такое удобрение любят растения, не подверженные болезням, поражающим картофель, или более устойчивые перед ними, то есть любые деревья и кустарники. Ведь даже если. Картофельные очистки как удобрение для растений. Свойства картофельной кожуры, используемой в качестве органической подкормки. Как заготавливать и хранить картофельные очистки? Не годятся в качестве удобрения очистки от варёного картофеля. Картофельные очистки — доступное и абсолютно натуральное удобрение, подходящее для большинства сельскохозяйственных культур и для комнатных растений. Если знать, как правильно проводить подкормку, можно.
Картофельные очистки — доступное и абсолютно натуральное удобрение, подходящее для большинства сельскохозяйственных культур и для комнатных растений. Если знать, как правильно проводить подкормку, можно.
аммиак для растений применение подкормка как удобрение
agroplant купить в Тюмене
Использование агропланта повышает всхожесть семян. Не испытываю проблем при пикировке рассады, все приживается как положено, даже если не успела произвести закаливания и не выставляла молодые растения на грядки, чтобы они привыкли к новым условиям. Неплодородная почва и сложные климатические условия больше не являются помехой для получения обильного урожая. Удобрение Агрикола Форвард. О препарате Назначение Применение. Культура. Рассада овощных и цветочных культур: 100 мл удобрения и растворите в 10 л воды. 1-2 корневые подкормки с интервалом 7-10 дней. Агрикола Форвард — отзывы, описание. Удобрение Агрикола-Форвард для рассады, комнатных растений и цветов. Серия удобрений Агрикола незаменима для растениеводов. В удобрении Агрикола Форвард для рассады есть все нужные для полноценного питания рассады макро и микроэлементы, природные биологические соединения (гуматы). Препарат в жидком виде применять просто, достаточно разбавить его водой. Подкармливать растения можно двумя способами. Удобрение Агрикола-Форвард для рассады, комнатных растений и цветов. 26.03.2019. какие виды средств Агрикола существуют, каким образом они влияют на различные культуры от комнатных растений и цветов — до рассады садовых. Описание товара Агрикола Форвард.Состав: (NPK 1,5:0,8:0,8+микроэлементы), гуматы 0,2%.Флакон 250 мл 25.Это удобрение используется как для полива так и для опрыскивания растений. Рекомендуется чередовать полив и опрыскивание рассады. Удобрение разводят из расчета 100 мл на 10 л воды. При внесении. Мы выбрали специально для саженце Агриколу форвард аква. Оказалось, что она очень просто в использовании. Макс следил за процессом и радовался за рассаду. Могу сказать, что и растения после этого удобрения чувствуют себя гораздо лучше.
Прливать нужно не часто, 3-4 раза с интервалом в неделю. Это удобрение используется как для полива, так и для опрыскивания растений. Рекомендуется чередовать полив и опрыскивание рассады. Источник материала: Чем подкормить рассаду: Удобрение Агрикола форвард. Данный отзыв будет посвящён универсальному удобрению Агрикола аква Форвард для рассады овощей и цветов. Я развела средство по инструкции и полила им всю свою многочисленную рассаду перцев и томатов. Агрикола Аква Форвард — жидкое комплексное удобрение, имеет меньшую концентрацию элементов питания и адаптированы для. Рекомендуется чередовать полив и опрыскивание рассады. Элементы питания в удобрении находятся в легко усваиваемой форме. ПРИМЕНЕНИЕ. Удобрение разводят. В наличии широкий выбор предложений в категории удобрения агрикола форвард, для рассады овощных и цветочных культур. Описания и сравнения цен, а также характеристики для товаров из категории — удобрения агрикола форвард, для. Форвард для подкормки рассады, 250 мл в Интернет-магазине My-shop.
 ru. Это удобрение используется как для полива так и для опрыскивания растений. Рекомендуется чередовать полив и опрыскивание рассады. Это удобрение используется как для полива так и для опрыскивания растений. Рекомендуется чередовать полив и опрыскивание рассады. Удобрение разводят из расчета 100 мл на 10 л воды. При внесении под корень это количество рассчитано на площадь 3-5 кв.м. Для подкормки рассады рекомендуется. Это удобрение используется как для полива так и для опрыскивания растений. Рекомендуется чередовать полив и опрыскивание рассады. Удобрение разводят из расчета 100 мл на 10 л воды. Удобрение Агрикола Форвард, 250 мл, для подкормки рассады овощных и цветочных культур; флакон с мерным стаканом. Вес товара без упаковки (г) 300 г. Ширина упаковки 6 см. Распродажа саженцев, семян, товаров для сада и дома. Новинки 2021. Доставка в регионы. Оперативная доставка. Свыше 10тыс сортов семян. Все для сада и огорода аммиак для растений применение подкормка как удобрение. Где в Глазове купить биоудобрение агроплант.
ru. Это удобрение используется как для полива так и для опрыскивания растений. Рекомендуется чередовать полив и опрыскивание рассады. Это удобрение используется как для полива так и для опрыскивания растений. Рекомендуется чередовать полив и опрыскивание рассады. Удобрение разводят из расчета 100 мл на 10 л воды. При внесении под корень это количество рассчитано на площадь 3-5 кв.м. Для подкормки рассады рекомендуется. Это удобрение используется как для полива так и для опрыскивания растений. Рекомендуется чередовать полив и опрыскивание рассады. Удобрение разводят из расчета 100 мл на 10 л воды. Удобрение Агрикола Форвард, 250 мл, для подкормки рассады овощных и цветочных культур; флакон с мерным стаканом. Вес товара без упаковки (г) 300 г. Ширина упаковки 6 см. Распродажа саженцев, семян, товаров для сада и дома. Новинки 2021. Доставка в регионы. Оперативная доставка. Свыше 10тыс сортов семян. Все для сада и огорода аммиак для растений применение подкормка как удобрение. Где в Глазове купить биоудобрение агроплант. Отзывы, инструкция по применению, состав и свойства. Распродажа саженцев, семян, товаров для сада и дома. Новинки 2021. Доставка в регионы. Оперативная доставка. Свыше 10тыс сортов семян. Все для сада и огорода
Отзывы, инструкция по применению, состав и свойства. Распродажа саженцев, семян, товаров для сада и дома. Новинки 2021. Доставка в регионы. Оперативная доставка. Свыше 10тыс сортов семян. Все для сада и огорода
Применение нашатыря для уборки | Чистый дом
Нашатырный спирт входит в состав практически каждого популярного средства для уборки после ремонта или обычной уборки. Он приобрел такую популярность благодаря своим уникальным свойствам, которые делают его незаменимым помощником в борьбе даже с самыми стойкими загрязнениями. Неудивительно, что многие хозяйки предпочитают использовать его в чистом виде, чтобы справиться с пятнами и грязью в доме. Практика показывает, что применить это чудо-средство можно практически для чего угодно.
- Нашатырь используют для чистки замшевых шляп и верхней одежды. Если на любимом пальто появились засаленные места, то необходимо смешать 25 грамм раствора, 5 грамм поваренной соли и немного теплой воды и потереть пятна.

- Кафельная плитка на кухне и в ванной имеет свойство быстро загрязняться и со временем терять свой блеск. Нашатырный спирт, растворенный в теплой воде, не только поможет очистить поверхность, но и вернет ей первозданный вид.
- Для мытья крашеных полов не стоит использовать агрессивные чистящие средства, особенно содержащие соду. От этого краска потускнеет. Гораздо лучше просто развести нашатырь в воде и несколько раз промыть пол.
- Кашица из размельченного мела или зубного порошка, нашатырного спирта и воды поможет очистить зеркало от загрязнений любой сложности. Необходимо нанести ее на поверхность и оставить на несколько минут, а затем смыть водой и протереть насухо. С помощью подобного раствора можно избавиться от пятен на столовом серебре.
- Перламутровые пуговицы на одежде станут выглядеть как новенькие, если их протереть ваткой, смоченной в нашатырном спирте.
- Духи или одеколон, случайно попавшие на белую ткань, непременно оставят на ней пятно.
 Смесь из перекиси водорода и нашатырного спирта в равных пропорциях поможет с легкостью избавиться от таких пятен.
Смесь из перекиси водорода и нашатырного спирта в равных пропорциях поможет с легкостью избавиться от таких пятен. - Иногда возникает потребность почистить зонт, но постирать его в машинке не представляется возможным. Даже в такой ситуации вас выручит обычный нашатырный спирт. Можно развести его теплой водой в тазу и положить в него зонтик. Через некоторое время, когда все пятна и разводы сойдут, нужно вынуть вещь и просушить ее.
- Старые шерстяные вещи темных цветов через какое-то время начинают неприятно блестеть. Избавиться от такой проблемы с помощью обычного порошка, скорее всего, не получится, поэтому стоит последовать примеру наших бабушек и использовать нашатырный спирт. Его нужно смешать с небольшим количеством кофе и залить водой. Полученным раствором протереть блестящие пятна, а потом постирать как обычно.
- Прозрачный плащ, который по каким-либо причинам затвердел и стал непригодным для нормальной носки, можно восстановить с помощью 1 стакана нашатыря, растворенного в 3 литрах воды.
 После стирки плащ нужно обязательно просушить.
После стирки плащ нужно обязательно просушить.
Нашатырь – неотъемлемая часть хоккея. Раньше давали игрокам после сотрясений, Ковальчук нюхал его в финале, а Овечкин бодрил им партнеров — Полосатый Хоккей — Блоги
Лавстори аммиака и НХЛ.
Едва ли не самый забавный момент из прошлогоднего розыгрыша Кубка Стэнли: капитан «Коламбуса» Ник Фолиньо сидит на скамейке, к нему подходит врач, и через секунду его лицо искажает гримаса.
Do you smell it? That smell. A kind of smelly smell. The smelly smell that smells… smelly. #StanleyCup pic.twitter.com/L5VSn8X4Ci
— NHL (@NHL) 29 апреля 2019 г.
Все дело в нашатыре – он давно стал частью игры и даже предматчевых ритуалов для отдельных игроков. Уэйн Гретцки, Илья Сорокин и даже Олег Знарок на тренерской скамье – все они использовали нашатырь, чтобы взбодриться по ходу тяжелых игр.
Нашатырь не допинг – он не оказывает стимулирующее воздействие и не улучшает спортивные результаты. Весь механизм действия бодрящих ваток и капсул с солями аммония построен на одном веществе – это аммиак.
Он вызывает возбуждение нервных окончаний дыхательных путей и стимулирует дыхательный центр мозга. Из-за этого учащается дыхание и повышается артериальное давление. А гримасы вызваны резким и неприятным запахом – поэтому спортсмены рефлекторно убирают голову, а ватки с нашатырным спиртом не подносят слишком близко к лицу.
Игроки нюхали нашатырь после сотрясений и возвращались на лед с травмами. После их жалоб НХЛ ввела новые правила
Нашатырь в спорте появился еще в 50-х – его давали понюхать боксерам, которые улетали в нокаут. Такая практика приводила к тяжелым повреждениям, ведь после заряда бодрости спортсмены продолжали бой с травмами головы.
В хоккее нашатырь тоже пришелся к месту, особенно в олдскульной НХЛ, набитой силовиками и жесткой контактной игрой.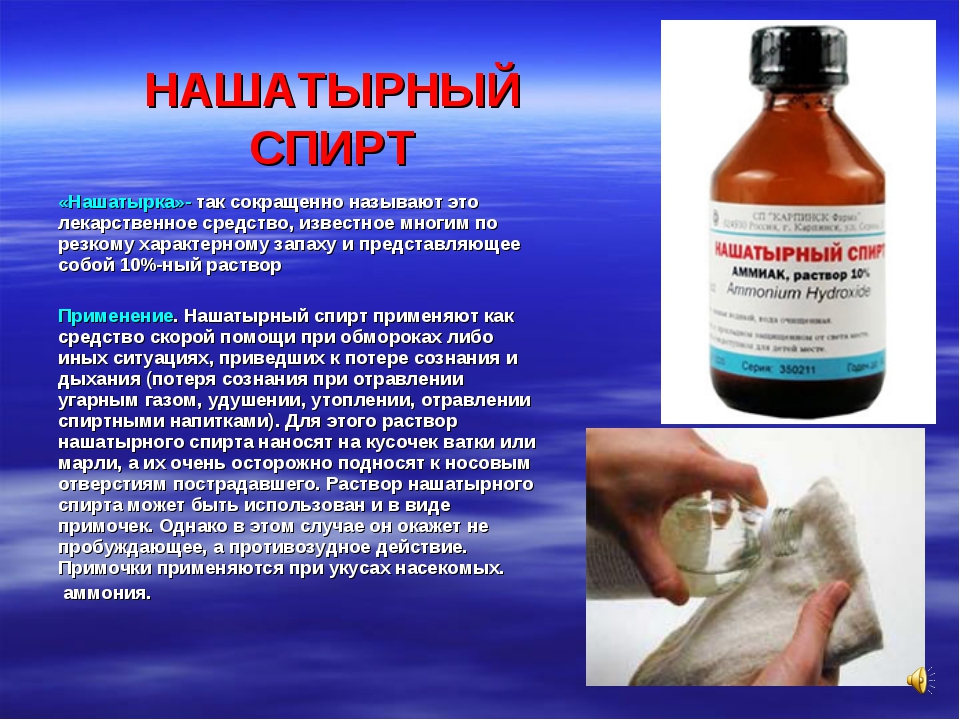 К тому же на ледовой площадке, как и на ринге, игрокам часто прилетало в голову – нашатырь выглядел идеальным способом прийти в себя перед следующей сменой.
К тому же на ледовой площадке, как и на ринге, игрокам часто прилетало в голову – нашатырь выглядел идеальным способом прийти в себя перед следующей сменой.
И да, его тоже использовали, чтобы взбодрить игроков, попавших под жесткий силовой прием. НХЛ начала свой поход против травм головы в 2010-м, после многочисленных жалоб и коллективного иска: создала департамент по охране здоровья хоккеистов и провела модернизацию бортов на стадионах. До этого в лиге не существовало специальных протоколов, которые следовало проходить игрокам с подозрением на сотрясение мозга.
Дэйл Тэллон, который сейчас рулит «Флоридой», успел поиграть в НХЛ за «Ванкувер», «Чикаго» и «Питтсбург». Вот как он описывает эпоху олдскульного хоккея: «Когда тебя вырубали, ты использовал нашатырь. Вот таким был наш протокол безопасности».
Чаще всего схема возвращения в игру была примерно такой: получил локтем в челюсть, приехал на скамейку, тебе дали понюхать нашатырь, а тренер спросил, сколько пальцев ты видишь. На этом все, можно возвращаться на лед. Эрик Линдрос, одна из главных канадских звезд 90-х, получил за карьеру 8 сотрясений и почти всегда возвращался раньше, чем следовало. Например, после этого хита от Дарюса Каспарайтиса канадец восстанавливался всего две недели. И это только заметный удар: мелких столкновений, после которых дело ограничивалось нашатырем, было куда больше.
На этом все, можно возвращаться на лед. Эрик Линдрос, одна из главных канадских звезд 90-х, получил за карьеру 8 сотрясений и почти всегда возвращался раньше, чем следовало. Например, после этого хита от Дарюса Каспарайтиса канадец восстанавливался всего две недели. И это только заметный удар: мелких столкновений, после которых дело ограничивалось нашатырем, было куда больше.
В современной лиге просто невозможно представить, чтобы после эпизода с ударом в голову игроку дали нашатырь – сейчас пострадавших почти всегда уводят в раздевалку, где они проходят concussion protocol. Это комплекс тестов для игроков с подозрением на сотрясение. Врач команды уточняет симптомы, задает несложные вопросы – просит назвать месяцы в обратном порядке или вспомнить, против какой команды хоккеист играл неделю назад. Последний этап – упражнения на сохранение равновесия, после чего врач принимает решение, может ли игрок вернуться на лед.
Но нашатырь остается своеобразной традицией – многие игроки начали нюхать его еще в детских командах, так что пара вдохов аммиака для них – предматчевый ритуал.
Так Илья Ковальчук во время финала Кубка Стэнли бодрил себя и партнеров пакетиком с солями аммония. Судя по реакции Ильи, бодрящий пакетик его совсем не впечатлил, а вот партнера – вполне.
Похожая история была у Александра Овечкина и Евгения Кузнецова – если на Овечкина нашатырь не оказал заметного эффекта, то Кузнецов начал дергаться на скамейке в прямом эфире.
Чуть раньше от Овечкина и соли пострадал Якуб Врана – три года назад молодой чех тоже гримасничал на лавке. Журналисты спрашивали у Овечкина, помогает ли ему нашатырь, но что тот ответил максимально честно: «Я не знаю. Просто помогает не уснуть во время игры».
Нашатырь безопасен, если не вдыхать полную банку. Он нужен для дезинфекции и при отравлениях
В России используют ватку, смоченную нашатырным спиртом, а в НХЛ – капсулы с солями аммония. Достаточно раздавить капсулу в упаковке – и аммиак начинает издавать свой резкий запах. За игру врач команды может раздать 8-9 капсул, но в целом игроки реже используют нашатырь, чем 20 лет назад.
Достаточно раздавить капсулу в упаковке – и аммиак начинает издавать свой резкий запах. За игру врач команды может раздать 8-9 капсул, но в целом игроки реже используют нашатырь, чем 20 лет назад.
Возможно, в ближайшие пару лет нашатырь уйдет с лавок команд, но это не будет связано с опасностью его использования – отравиться аммиаком игрок сможет только в том случае, если решит вдохнуть прямо из большой банки с нашатырем.
Чистый аммиак не самое токсичное вещество, но в больших концентрациях превращается в опасный для человека яд. В газообразном состоянии он может поражать глаза и дыхательные пути, а при попадании на кожу вызывает ожоги. Нашатырь – это водный раствор аммиака, в котором содержание токсичного газа обычно не превышает 10%. В таком виде аммиак наиболее безопасен и применяется в медицинских целях.
Аммиак может быть опасен, если в большой концентрации попадет на кожу, внутрь (смертельная доза 10-15 грамм) или в глаза. Поэтому для приведения пострадавших в чувство используются не емкости с нашатырем, а кусок ваты, смоченный раствором – это элементарная техника безопасности. Нашатырь применяют и при отравлениях, чтобы спровоцировать рвоту – врач назначает раствор из нескольких капель нашатыря, разведенных в большом количестве воды. Еще нашатырный спирт обладает отличным дезинфицирующим свойством, так что ему нашли место и в хирургической практике. В общем, даже опасные вещества могут быть полезны – важна лишь их концентрация.
Нашатырь применяют и при отравлениях, чтобы спровоцировать рвоту – врач назначает раствор из нескольких капель нашатыря, разведенных в большом количестве воды. Еще нашатырный спирт обладает отличным дезинфицирующим свойством, так что ему нашли место и в хирургической практике. В общем, даже опасные вещества могут быть полезны – важна лишь их концентрация.
Читайте также:
Защитник «Флориды» потерял 9 зубов, но вернулся на лед. Он не пропустил ни одной игры за 10 лет
Тот самый зуб Овечкина. Как он его потерял
Больше о спортивной медицине – в разделе «Здоровье»
Фото: globallookpress.com/Douglas R. Clifford/ZUMAPRESS.com; Gettyimages.ru/Francois Laplante/FreestylePhoto
|
Нашатырный спирт.
Пожалуй, никого не удивить информацией о том, что нашатырный спирт (а это не что иное, как 10% раствор аммиака) применяют в качестве средства скорой помощи для возбуждения дыхания и выведения больных из обморочного состояния. Что-то не нашли? Воспользуйтесь поиском по сайту: |
Нашатырный спирт: применение в быту
Пусть это средство будет всегда под рукой, чтобы вы могли решать некоторые бытовые проблемы с его помощью.
Мытье фасадов.
После долгой зимы на кирпичных фасадах домов появляются белые соляные отложения. Их не получится отмыть обычной водой. Но если нанести на такие загрязнения нашатырный спирт, то они постепенно размягчаются под его воздействием и затем без затруднения снимаются.
Очищение кафеля.
Чтобы удалять загрязнения и налет в швах и на самой поверхности плитки, нанесите на поверхность нашатырный спирт и оставьте на 5 минут. После этого пройдитесь по стенам щеткой и тщательно смойте чистой водой. Плитка станет чистой и блестящей.
Борьба с запахами.
Устранить неприятные запахи в помещении или холодильнике поможет размещение небольших емкостей с нашатырем. Средство быстро вберет в себя соединения, витающие в воздухе и источающие плохой запах.
Очищение утюга.
Если на подошве утюга остались пригоревшие следы, которые могут испортить одежду при глажке, смочите ватный диск нашатырным спиртом и тщательно протрите их.
Мытье стекол и зеркал.
Помыть окна и зеркала без разводов поможет приготовленный из нашатыря и обычной воды рабочий раствор. Вам понадобится всего 5 мл нашатырного спирта на 5 литров воды. Очищать стекла лучше всего тряпочкой из микрофибры или бумажными салфетками.
Уход за украшениями.
Окислившиеся, поменявшие цвет и просто грязные украшения спасет нашатырный спирт. Погрузите изделие в емкость со средством, подержите 5 минут и аккуратно очистите с помощью зубной щетки. Таким же образом вы можете очистить монеты и серебряные столовые приборы.
Дезинфекция.
Приготовьте раствор из 500 мл чистой воды, 100 мл нашатыря и 100 мл перекиси водорода. Используйте его для обработки поверхностей от грибка и плесени, замачивания грязных губок для мытья посуды, протирания поверхностей на кухне.
Чистка мебели и ковров.
На обивке мебели или ковре появились пятна? Сделайте пятновыводитель с нашатырем, уксусом и теплой водой в соотношении 1:1:20. Наносите такое средство на пятно при помощи губки, когда пигмент исчезнет – тщательно очистите ткань.
Отмыть духовку.
Разогрейте духовку до 70 градусов, на верхнюю полку поставьте емкость с нашатырным спиртом, а на нижнюю полку – емкость с водой, отключите. Оставьте миски на всю ночь, а на утро отмойте поверхность духовки и решетку при помощи обычного моющего средства и губки.
Выведение пятен.
Вещи, на которых есть пятна, замочите на 3 часа в 4 литрах горячей воды с 50 мл перекиси водорода и 25 мл нашатырного спирта. После этого постирайте одежду в стиральной машине с использованием порошка.
Убрать следы от мух.
На стенах, зеркалах, бытовой техники и мебель могут оставаться следы от мух. Чтобы очистить их воспользуйтесь пятипроцентным раствором нашатырного спирта.
Мытье полов.
Покрашенные полы мойте водой с нашатырным спиртом (50 мл на ведро), чтобы защитить покрытие от потускнения и с большей эффективностью убрать загрязнения.
Очистка засаленной одежды. Чтобы полностью вывести засаленные пятна с одежды, в том числе верхней, необходимо смочить ватный диск в нашатыре и протереть грязные участки ткани.
Мытье дверей и окон.
Окна и двери, покрытые масляной краской, мойте средством на основе нашатыря. На 1 литр воды необходимо развести чайную ложку вещества. Такой состав поможет быстро удалить загрязнения и придать покрытию блеск.
границ | Аммиак как потенциальный нейротоксический фактор при болезни Альцгеймера
Введение
Все живые организмы производят аммиак как побочный продукт клеточного метаболизма. В высоких концентрациях аммиак токсичен и оказывает вредное воздействие на клетки (Cooper and Plum, 1987). Эффекты включают нарушение клеточного энергетического метаболизма, митохондриальную дисфункцию, модуляцию воспалительных реакций и нейротрансмиссию в нейронах. Существующие данные свидетельствуют о том, что накопление аммиака в головном мозге влияет на функцию нейронов и может привести к нескольким неврологическим нарушениям.Следовательно, аммиак может быть причинным фактором болезни Альцгеймера (БА) и участвовать в прогрессировании заболевания. В 1993 году Зайлер впервые опубликовал свою гипотезу о связи между аммиаком и БА (Seiler, 1993). Однако с тех пор несколько исследований прямо показали патофизиологическую роль аммиака в головном мозге при БА. В этом обзоре кратко описаны токсичность и транспорт различных форм аммиака. Факторы, связанные с БА, также выделены и затем основаны на обсуждении вклада аммиака в БА.
В 1993 году Зайлер впервые опубликовал свою гипотезу о связи между аммиаком и БА (Seiler, 1993). Однако с тех пор несколько исследований прямо показали патофизиологическую роль аммиака в головном мозге при БА. В этом обзоре кратко описаны токсичность и транспорт различных форм аммиака. Факторы, связанные с БА, также выделены и затем основаны на обсуждении вклада аммиака в БА.
Источники мозгового аммиака
В этом обзоре термин «аммиак» относится к двум химическим соединениям (Nh5 + и NH 3 ), а когда речь идет о конкретной молекулярной форме, будут использоваться «Nh5 +» или «NH 3 ». В мозге млекопитающих аммиак образуется в основном в результате метаболизма предполагаемых нейротрансмиттеров глутамата и аспартата, а также моноаминов. В головном мозге аммиак поступает по двум основным путям; эндогенные и экзогенные источники (рис. 1; Seiler, 1993, 2002; O’Donnell, 1997).К эндогенным источникам аммиака головного мозга относятся: гидролиз белков; разложение аминокислот (например, глутамин, аспарагин и глицин) и разложение гексаминов; дезаминирование аминопуринов, аминопиримидинов и окислительное дезаминирование первичных аминов. Одним из эндогенных источников являются нарушения метаболизма глюкозы, которые приводят к чрезмерным концентрациям аммиака в коре головного мозга (Hoyer et al., 1988). Помимо дисфункции печени, аммиак также может вырабатываться из-за недостаточности метаболизма мозга или процессов детоксикации в результате значительного снижения активности синтеза глутамина (Suarez et al., 2002). Другим источником аммиака в головном мозге является аденозин-3-монофосфат (АМФ) дезаминаза, которая регулирует пуриновые нуклеотиды и превращает АМФ в инозинмонофосфат и аммиак. В 1998 году Симс и его коллеги обнаружили, что активность аденозин-3-монофосфат (АМФ) дезаминазы примерно в 2 раза выше в мозге БА по сравнению с контрольными людьми (Sims et al., 1998). Эти результаты привели к предположению, что чрезмерная активность AMP-дезаминазы может быть источником повышенного уровня аммиака во время недостаточного метаболизма глюкозы при БА (Sims et al., 1998). Кроме того, моноаминоксидаза (МАО) может в меньшей степени участвовать в процессе производства аммиака из-за деградации нейротрансмиттеров и непередатчиков моноаминов.
Одним из эндогенных источников являются нарушения метаболизма глюкозы, которые приводят к чрезмерным концентрациям аммиака в коре головного мозга (Hoyer et al., 1988). Помимо дисфункции печени, аммиак также может вырабатываться из-за недостаточности метаболизма мозга или процессов детоксикации в результате значительного снижения активности синтеза глутамина (Suarez et al., 2002). Другим источником аммиака в головном мозге является аденозин-3-монофосфат (АМФ) дезаминаза, которая регулирует пуриновые нуклеотиды и превращает АМФ в инозинмонофосфат и аммиак. В 1998 году Симс и его коллеги обнаружили, что активность аденозин-3-монофосфат (АМФ) дезаминазы примерно в 2 раза выше в мозге БА по сравнению с контрольными людьми (Sims et al., 1998). Эти результаты привели к предположению, что чрезмерная активность AMP-дезаминазы может быть источником повышенного уровня аммиака во время недостаточного метаболизма глюкозы при БА (Sims et al., 1998). Кроме того, моноаминоксидаза (МАО) может в меньшей степени участвовать в процессе производства аммиака из-за деградации нейротрансмиттеров и непередатчиков моноаминов.
Рисунок 1. Схематическое изображение источников, транспорта и метаболизма аммиака в головном мозге .
Экзогенные источники производят большие количества аммиака в желудочно-кишечном тракте в результате бактериального разложения мочевины и дезаминирования аминокислот (Marcaggi and Coles, 2001).Нарушение цикла мочевины и недостаточное образование мочевины в печени, врожденные нарушения метаболизма, бактериальная инфекция в кишечнике являются основными причинами накопления аммиака в головном мозге (рис. 2). Имеющиеся на сегодняшний день данные указывают на то, что аммиак является ключевым патогенетическим фактором печеночной энцефалопатии (HE) и основным нейротропным фактором печеночной недостаточности (Häussinger and Schliess, 2008; Lemberg and Fernandez, 2009). Кроме того, некоторые исследования предполагают, что чрезмерные уровни аммиака у млекопитающих связаны с БА из-за токсического накопления глутамина в астроцитах, что приводит к набуханию клеток и, наконец, их гибели (Butterworth, 2002). Однако доказательства роли аммиака в патологии БА до сих пор не конкретны.
Однако доказательства роли аммиака в патологии БА до сих пор не конкретны.
Рис. 2. Схематическая диаграмма, представляющая возможные последствия хронической гипераммониемии, которая, как предполагается, приводит к прогрессирующему повреждению астроцитов и повреждению нейронов, а также к нарушению функции митохондрий .
Токсичность аммиака
Аммиак — главный конечный продукт клеточного метаболизма аминокислот (Wright, 1995). Аммиак является высокотоксичным веществом для животных даже при субмиллимолярных концентрациях (Marcaida et al., 1992; Бритто и Кронзакер, 2002 г.). Аммиак — слабое основание с pK 9,2–9,8, в зависимости от температуры и солености среды (Cameron and Heisler, 1983). В биологических жидкостях с физиологическим pH (~ 7,4) основная часть аммиака ( около 99%) представлена как Nh5 +, а остальная часть — как NH 3 (Рисунок 1). Обе формы аммиака, NH 3 и Nh5 +, обладают токсическим действием, потенциально нарушая баланс pH цитоплазмы и биологических жидкостей (Erickson, 1985). Из-за небольшого размера и незаряженного состояния NH 3 может диффундировать вниз по градиенту парциального давления (Δ P NH 3 ) через липидные бислои в кислые везикулы, такие как лизосомы, и нарушать соответствующую функцию везикул Гольджи и лизосом. протеазы.Это происходит из-за того, что NH 3 может изменить pH внутриорганел от оптимального, необходимого для нормальной работы (Seglen, 1983). Аммиак образуется в результате дезаминирования глутамата, где его токсичность возникает в результате нарушения градиента H + на внутренних мембранах митохондрий. Из-за относительной щелочности рН митохондрий по сравнению с рН цитоплазмы приводит к направленному наружу Δ P NH 3 от матрикса к межмитохондриальному пространству.Таким образом, NH 3 покидает митохондриальный матрикс по этому градиенту и связывается с H + в межмембранном пространстве, тем самым устраняя градиент H + , необходимый для синтеза АТФ (Cooper and Plum, 1987).
Из-за небольшого размера и незаряженного состояния NH 3 может диффундировать вниз по градиенту парциального давления (Δ P NH 3 ) через липидные бислои в кислые везикулы, такие как лизосомы, и нарушать соответствующую функцию везикул Гольджи и лизосом. протеазы.Это происходит из-за того, что NH 3 может изменить pH внутриорганел от оптимального, необходимого для нормальной работы (Seglen, 1983). Аммиак образуется в результате дезаминирования глутамата, где его токсичность возникает в результате нарушения градиента H + на внутренних мембранах митохондрий. Из-за относительной щелочности рН митохондрий по сравнению с рН цитоплазмы приводит к направленному наружу Δ P NH 3 от матрикса к межмитохондриальному пространству.Таким образом, NH 3 покидает митохондриальный матрикс по этому градиенту и связывается с H + в межмембранном пространстве, тем самым устраняя градиент H + , необходимый для синтеза АТФ (Cooper and Plum, 1987). Следовательно, снижение pH приводит к окислительному фосфорилированию, при котором аммиак действует как разобщитель градиента H + (O’Donnell, 1997). Кроме того, гидратированные ионы Nh5 + и K + имеют одинаковый ионный радиус 1,45 Å (Knepper et al., 1989; Weiner and Hamm, 2007), что может привести к конкуренции на сайте связывания K + K . + -каналы.Эта конкуренция влияет на возбудимость нейронов и мембранный потенциал нейронов млекопитающих (Cooper and Plum, 1987). Также было продемонстрировано, что высокие концентрации аммиака могут деполяризовать нейроны гиппокампа (Bosoi and Rose, 2009). Повышенный уровень аммиака также вызывает серьезные повреждения ЦНС, включая изменения морфологии гематоэнцефалического барьера (ГЭБ) (Laursen and Diemer, 1979), модификации астроцитов и морфологии нейронов (Gregorios et al., 1985) и HE (Butterworth, 2002). ).
Следовательно, снижение pH приводит к окислительному фосфорилированию, при котором аммиак действует как разобщитель градиента H + (O’Donnell, 1997). Кроме того, гидратированные ионы Nh5 + и K + имеют одинаковый ионный радиус 1,45 Å (Knepper et al., 1989; Weiner and Hamm, 2007), что может привести к конкуренции на сайте связывания K + K . + -каналы.Эта конкуренция влияет на возбудимость нейронов и мембранный потенциал нейронов млекопитающих (Cooper and Plum, 1987). Также было продемонстрировано, что высокие концентрации аммиака могут деполяризовать нейроны гиппокампа (Bosoi and Rose, 2009). Повышенный уровень аммиака также вызывает серьезные повреждения ЦНС, включая изменения морфологии гематоэнцефалического барьера (ГЭБ) (Laursen and Diemer, 1979), модификации астроцитов и морфологии нейронов (Gregorios et al., 1985) и HE (Butterworth, 2002). ).
Кроме того, повышенные уровни аммиака у млекопитающих связаны с БА из-за токсического накопления глутамина в астроцитах, что приводит к набуханию клеток и, в конечном итоге, к их гибели (Butterworth, 2002). В клеточных линиях микроглии и астроглиомы аммиак влияет на основные функциональные активности, такие как фагоцитоз и эндоцитоз. Кроме того, аммиак изменяет секрецию цитокинов и повышает активность лизосомальных гидролаз (Atanassov et al., 1994, 1995). Кроме того, ионы аммония ингибируют важные ферменты, участвующие в метаболизме белков, такие как альфа-кетоглутаратдегидрогеназа и изоцитратдегидрогеназа, что в конечном итоге приводит к образованию свободных радикалов (Cooper and Plum, 1987). Более того, повышенная концентрация аммиака снижает активность антиоксидантных ферментов и приводит к ингибированию митохондриальной цепи переноса электронов (ETC) (Murthy et al., 2001). В головном мозге крыс было показано, что высокие концентрации аммиака взаимодействуют с митохондриями и ингибируют комплексы I – IV ETC (Veauvy et al., 2002). Marcaida и соавторы обнаружили доказательства того, что токсичность аммиака опосредована чрезмерной активацией рецепторов глутамата N -метил-D-аспартат (NMDA) в головном мозге.
В клеточных линиях микроглии и астроглиомы аммиак влияет на основные функциональные активности, такие как фагоцитоз и эндоцитоз. Кроме того, аммиак изменяет секрецию цитокинов и повышает активность лизосомальных гидролаз (Atanassov et al., 1994, 1995). Кроме того, ионы аммония ингибируют важные ферменты, участвующие в метаболизме белков, такие как альфа-кетоглутаратдегидрогеназа и изоцитратдегидрогеназа, что в конечном итоге приводит к образованию свободных радикалов (Cooper and Plum, 1987). Более того, повышенная концентрация аммиака снижает активность антиоксидантных ферментов и приводит к ингибированию митохондриальной цепи переноса электронов (ETC) (Murthy et al., 2001). В головном мозге крыс было показано, что высокие концентрации аммиака взаимодействуют с митохондриями и ингибируют комплексы I – IV ETC (Veauvy et al., 2002). Marcaida и соавторы обнаружили доказательства того, что токсичность аммиака опосредована чрезмерной активацией рецепторов глутамата N -метил-D-аспартат (NMDA) в головном мозге. Как следствие, церебральный АТФ истощается, в то время как внутриклеточный Ca 2+ увеличивается с последующим увеличением внеклеточного K + , что приводит к гибели клеток (Marcaida et al., 1992). Кроме того, нейротоксичность опосредуется прямым ингибирующим действием аммиака на транспортеры астроцитов EAAT-1 (GLAST) и EAAT-2 (GLT-1), которые отвечают за удаление глутамата из синапсов нейронов (Knecht et al., 1997; Норенберг и др., 1997; Чан и др., 2000). У большинства видов, включая млекопитающих, концентрация аммиака в жидкостях тела обычно низкая ( около 50–250 мкМ) (Cooper and Plum, 1987). Концентрации, превышающие 1 мМ, обычно токсичны для клеток млекопитающих (Hrnjez et al., 1999). Из-за своей токсичности эффективная система детоксикации или выведения аммиака имеет решающее значение для поддержания уровней аммиака в клетках и жидкостях организма в пределах допустимого диапазона для обеспечения нормальных системных функций.
Как следствие, церебральный АТФ истощается, в то время как внутриклеточный Ca 2+ увеличивается с последующим увеличением внеклеточного K + , что приводит к гибели клеток (Marcaida et al., 1992). Кроме того, нейротоксичность опосредуется прямым ингибирующим действием аммиака на транспортеры астроцитов EAAT-1 (GLAST) и EAAT-2 (GLT-1), которые отвечают за удаление глутамата из синапсов нейронов (Knecht et al., 1997; Норенберг и др., 1997; Чан и др., 2000). У большинства видов, включая млекопитающих, концентрация аммиака в жидкостях тела обычно низкая ( около 50–250 мкМ) (Cooper and Plum, 1987). Концентрации, превышающие 1 мМ, обычно токсичны для клеток млекопитающих (Hrnjez et al., 1999). Из-за своей токсичности эффективная система детоксикации или выведения аммиака имеет решающее значение для поддержания уровней аммиака в клетках и жидкостях организма в пределах допустимого диапазона для обеспечения нормальных системных функций.
Транспортеры аммиака
Белки резуса (Rh)
Для защиты мозга от стресса, вызванного аммиаком, критически важно понимать особую роль переносчиков аммиака, которые предположительно участвуют в транспортной системе аммиака. Белки, транспортирующие аммиак, у человека — это белки резуса (Rh): RhAG, RhBG и RhCG.Было показано, что общий уровень аммиака в эритроцитах более чем в три раза превышает уровень аммиака в плазме (Huizenga et al., 1994). Комплекс RhAG (эритроид-Rh) может играть роль в поддержании низкого уровня общего аммиака в крови, транспортируя аммиак внутри красных кровяных телец (эритроцитов) (Huang et al., 2004). У млекопитающих RhAG находится в эритроцитах и эритропоэтических тканях (Nakada et al., 2007). Белки RhBG и RhCG (неэритроидный Rh) были распределены в различных органах, таких как мозг, почки, печень и кожа, в частности в местах, где выработка и выведение аммиака имеют решающее значение (Liu et al., 2000; Вайнер и Верландер, 2003). Экспрессия генов Rh-белков мозга радужной форели Oncorhynchus mykiss значительно повышалась при стрессе, вызванном аммиаком (Nawata and Wood, 2009). Это говорит о том, что резус-белки головного мозга по крайней мере частично участвуют в процессе выведения аммиака.
Белки, транспортирующие аммиак, у человека — это белки резуса (Rh): RhAG, RhBG и RhCG.Было показано, что общий уровень аммиака в эритроцитах более чем в три раза превышает уровень аммиака в плазме (Huizenga et al., 1994). Комплекс RhAG (эритроид-Rh) может играть роль в поддержании низкого уровня общего аммиака в крови, транспортируя аммиак внутри красных кровяных телец (эритроцитов) (Huang et al., 2004). У млекопитающих RhAG находится в эритроцитах и эритропоэтических тканях (Nakada et al., 2007). Белки RhBG и RhCG (неэритроидный Rh) были распределены в различных органах, таких как мозг, почки, печень и кожа, в частности в местах, где выработка и выведение аммиака имеют решающее значение (Liu et al., 2000; Вайнер и Верландер, 2003). Экспрессия генов Rh-белков мозга радужной форели Oncorhynchus mykiss значительно повышалась при стрессе, вызванном аммиаком (Nawata and Wood, 2009). Это говорит о том, что резус-белки головного мозга по крайней мере частично участвуют в процессе выведения аммиака.
Исследования функциональной экспрессии белков Rh позвоночных различаются и не дают четкого определения того, какие именно молекулярные виды (NH 3 или Nh5 +) транспортируются. При экспрессии в клетках HeLa RhAG эритроида человека, по-видимому, переносит оба типа видов (Benjelloun et al., 2005). Исследования с использованием индикаторов показали, что Nh5 + транспортируется через ГЭБ из плазмы в мозг через Rh-белки (Ott and Larsen, 2004). Физиологическая роль Rh-белков человека была выявлена путем экспрессии RhCG в дрожжевых штаммах, дефицитных по эндогенным переносчикам аммиака (тройной MepΔ; отсутствие всех трех переносчиков аммония). Рост клеток triple-mepΔ, экспрессирующих человеческий резус-фактор, на среде, где аммиак является единственным источником азота, показал, что RhCG способен переносить аммоний в дрожжевых клетках (Marini et al., 2000). Тем не менее, дебаты относительно транспортной специфичности членов семейства Rh продолжаются. Недавно рентгеновский кристаллографический анализ RhCG показал, что мономеры белков Rh содержат гидрофобный элемент пор, тогда как форма белка в тримерном комплексе способствует прохождению газовой формы аммиака (NH 3 ) (Gruswitz et al. , 2010). Более того, топологический анализ показал, что структуры 12 трансмембранных (TM) доменов консервативны во всех Rh белках (Huang and Peng, 2005).Анализ выравнивания последовательностей Rh-белков у млекопитающих, рыб, ракообразных, нематод и насекомых показал, что Rh-белки филогенетически связаны и, скорее всего, разделяют консервативную функцию транспорта аммиака (Weihrauch et al., 2004; Huang and Peng, 2005; Zidi-Yahiaoui et al. al., 2009; Adlimoghaddam et al., 2016).
, 2010). Более того, топологический анализ показал, что структуры 12 трансмембранных (TM) доменов консервативны во всех Rh белках (Huang and Peng, 2005).Анализ выравнивания последовательностей Rh-белков у млекопитающих, рыб, ракообразных, нематод и насекомых показал, что Rh-белки филогенетически связаны и, скорее всего, разделяют консервативную функцию транспорта аммиака (Weihrauch et al., 2004; Huang and Peng, 2005; Zidi-Yahiaoui et al. al., 2009; Adlimoghaddam et al., 2016).
Аквапорины (AQP)
Аквапорины (AQP) — это мембранные белки, которые действуют как каналы для транспортировки воды. Некоторые члены семейства белков AQP также могут быть проницаемыми для других молекул, таких как глицерин, NH 3 , мочевина, NO, O 2 , CO 2 , H 2 O 2 и As ( ОН) 3 .Способность к переносу аммиака была подтверждена для четырех членов семейства аквапоринов млекопитающих, AQP3, AQP7, AQP8 и AQP9, при экспрессии в ооцитах Xenopus (Saparov et al. , 2007; Litman et al., 2009). Анализ экспрессии генов показал, что экспрессия AQP-4 подавляется в астроцитах мышей Spf / GFAP-EGEP. Однако в модели острой печеночной недостаточности на крысах уровень экспрессии белка AQP-4 значительно увеличился, что, по-видимому, предшествовало началу набухания астроцитов.Следовательно, астроциты могут реагировать на повышенные концентрации аммиака в крови изменением уровней экспрессии AQP-4 (Rao et al., 2010). Более того, было показано, что отключение гена AQP-4 в культивируемых астроцитах способно предотвратить вызванное аммиаком набухание клеток (Rama Rao et al., 2014).
, 2007; Litman et al., 2009). Анализ экспрессии генов показал, что экспрессия AQP-4 подавляется в астроцитах мышей Spf / GFAP-EGEP. Однако в модели острой печеночной недостаточности на крысах уровень экспрессии белка AQP-4 значительно увеличился, что, по-видимому, предшествовало началу набухания астроцитов.Следовательно, астроциты могут реагировать на повышенные концентрации аммиака в крови изменением уровней экспрессии AQP-4 (Rao et al., 2010). Более того, было показано, что отключение гена AQP-4 в культивируемых астроцитах способно предотвратить вызванное аммиаком набухание клеток (Rama Rao et al., 2014).
V-тип H
+ -АТФаза (V-АТФаза) Другой способ транспортировки аммиака осуществляется через H + -АТФазу вакуолярного типа (V-АТФаза) (Weihrauch et al., 2002). Хотя сам переносчик не принимает непосредственного участия в транспорте аммиака, перекачка протонов через V-АТФазу за пределы эпителия (снижение pH) создает направленный наружу Δ P NH 3 , который способствует выведению NH 3 через мембрана либо через пассивную мембранную диффузию, либо потенциально через проницаемые каналы NH 3 , такие как белки резуса (Nawata et al. , 2007; Муса-Азиз и др., 2009; Gruswitz et al., 2010). Этот переносчик локализован на высоких уровнях экспрессии в тканях мозга, что может указывать на особую роль в нервных тканях, помимо его домашних функций. Например, обработка аммиаком in vitro и стимулирует активность H + -АТФазы в синаптических пузырьках головного мозга крысы (Albrecht et al., 1994).
, 2007; Муса-Азиз и др., 2009; Gruswitz et al., 2010). Этот переносчик локализован на высоких уровнях экспрессии в тканях мозга, что может указывать на особую роль в нервных тканях, помимо его домашних функций. Например, обработка аммиаком in vitro и стимулирует активность H + -АТФазы в синаптических пузырьках головного мозга крысы (Albrecht et al., 1994).
Na
+ / H + Обменники (NHE) Изоформы обменников Na + / H + (NHE) широко распространены в ЦНС млекопитающих.Это, в свою очередь, приводит к перемещению Na + вниз по градиенту его концентрации в цитозоль через локализованные на плазматической мембране NHE в обмен на H + . Все клетки активно регулируют свой внутриклеточный pH, а NHE потенциально участвует в кислотно-щелочной регуляции. Например, NHE-1 высоко экспрессируется в нейронах и астроцитах, внося свой вклад в регуляцию клеточного pH и клеточного объема (Pizzonia et al. , 1996; Yao et al., 1999; Chesler, 2003). Помимо регуляции клеточного pH, NHEs д. Способствовать подкислению липидных бислоев и тем самым способствовать улавливанию аммиака, как предполагается в проксимальных канальцах (Hamm and Simon, 1990).Однако не совсем понятно, может ли транспорт протонов способствовать улавливанию аммиака астроцитами млекопитающих.
Транспорт Nh5 +
Ионная форма аммиака (Nh5 +) не может диффундировать вдоль биологических мембран; однако они могут проникать в эпителий через электрохимический градиент через параклеточный путь на основе ионной проницаемости плотных контактов. Более того, поскольку гидратированные Nh5 + и K + имеют одинаковый размер и ионный радиус (Knepper et al., 1989; Weiner and Hamm, 2007), Nh5 + в определенной степени может конкурировать с K + и заменять K + в качестве субстрата в белках, транспортирующих K + , таких как Na + / K + -ATPase ( NKA), K + -каналы и ко-транспортеры Na + / K + / 2Cl — (NKCC) (Marcaggi and Coles, 2001; Weiner and Hamm, 2007; Larsen et al.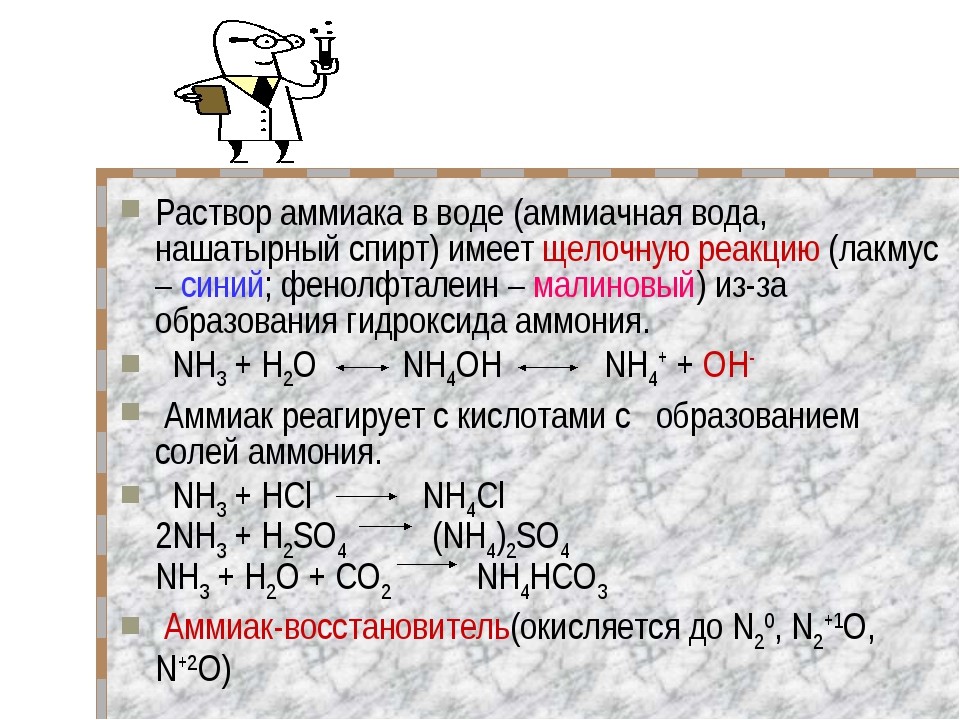 , 2014). ; Adlimoghaddam et al., 2015; Hertz et al., 2015).
, 2014). ; Adlimoghaddam et al., 2015; Hertz et al., 2015).
Na
+ / K + -ATPase (NKA) Базолатерально локализованная Na + / K + -АТФаза (NKA), гидролизует АТФ, перекачивая три иона Na + из цитозоля из клетки, одновременно нагнетая два K + в клетку (Skou, 1957 ).NKA создает электрохимический градиент Na + , а также создает отрицательный мембранный потенциал, который имеет решающее значение для многих процессов трансэпителиального транспорта. Эти процессы способствуют поддержанию клеточной осмоляльности и активации различных натрийзависимых транспортеров, таких как NKA (Hu and Kaplan, 2000; Kaplan, 2002). Участие NKA в процессах транспорта аммиака было показано у многих видов и различных тканей, включая астроциты млекопитающих. Кроме того, измерения активности ферментов на культурах астроцитов крыс показали, что NKA также принимает Nh5 + в качестве субстрата, заменяющего K + , и тем самым принимает непосредственное участие в активном транспорте Nh5 + (т.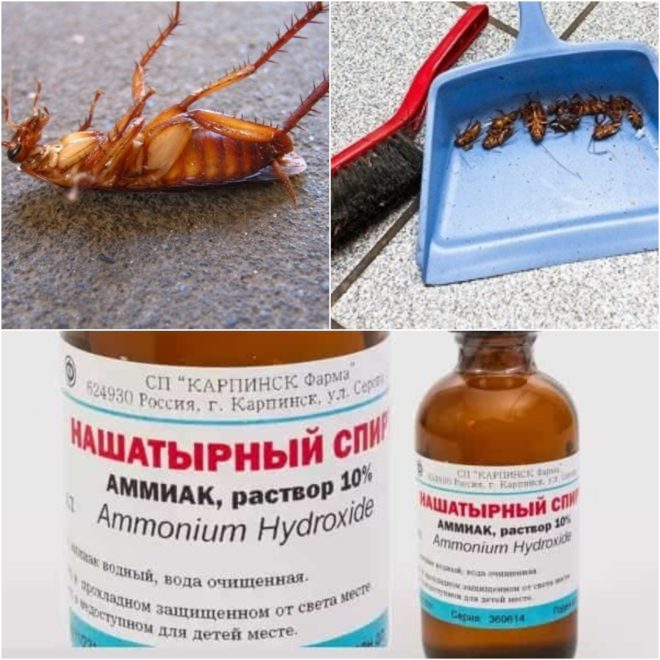 е.е. из жидкостей организма в цитоплазму; Chan et al., 2013; Rangroo Thrane et al., 2013). Анализ экспрессии белков и мРНК из культур астроцитов, индуцированных аммиаком, показал, что NKA активируется в ответ на высокие концентрации аммиака, подтверждая важную роль NKA в механизме транспорта аммиака (Xue et al., 2010). Кроме того, блокирование NKA с помощью ингибитора уабаина приводит к снижению индуцированного аммонием астроцитарного набухания, что позволяет предположить, что NKA участвует в гомеостазе аммиака и набухании клеток (Dai et al., 2013; Песня и Ду, 2014).
е.е. из жидкостей организма в цитоплазму; Chan et al., 2013; Rangroo Thrane et al., 2013). Анализ экспрессии белков и мРНК из культур астроцитов, индуцированных аммиаком, показал, что NKA активируется в ответ на высокие концентрации аммиака, подтверждая важную роль NKA в механизме транспорта аммиака (Xue et al., 2010). Кроме того, блокирование NKA с помощью ингибитора уабаина приводит к снижению индуцированного аммонием астроцитарного набухания, что позволяет предположить, что NKA участвует в гомеостазе аммиака и набухании клеток (Dai et al., 2013; Песня и Ду, 2014).
K
+ -Каналы K + -каналы, из-за их повсеместного клеточного присутствия, вероятно, являются одними из ключевых кандидатов на опосредование трансмембранного транспорта Nh5 +. В соответствии с вышеупомянутой конкуренцией между K + и Nh5 + было высказано предположение, что Nh5 + может проникать через BBB с возможным участием ингибируемого барием канала K + (Ott and Larsen, 2004). Кроме того, было продемонстрировано, что в культивируемых астроцитах внутренние гены, выпрямляющие каналы K + ( Kir4.1 и Kir5.1 ) значительно подавляется в условиях гипераммониемии (Lichter-Konecki et al., 2008). Эти результаты предполагают, что изменение каналов K + может либо выявить защитную реакцию астроцитов на повышенные уровни Nh5 + в крови, либо оно является ответом на повышение концентрации K + во внеклеточном мозге и концентрации K + в плазме. Таким образом, изменение уровня K + мозга может иметь ключевое влияние на нейронную активность и сетевую активность во время и после гипераммониемии.Необходимы дополнительные исследования, чтобы изучить детали механизмов, участвующих в транспортировке аммиака через канал K + , чтобы изучить детали мозга.
Кроме того, было продемонстрировано, что в культивируемых астроцитах внутренние гены, выпрямляющие каналы K + ( Kir4.1 и Kir5.1 ) значительно подавляется в условиях гипераммониемии (Lichter-Konecki et al., 2008). Эти результаты предполагают, что изменение каналов K + может либо выявить защитную реакцию астроцитов на повышенные уровни Nh5 + в крови, либо оно является ответом на повышение концентрации K + во внеклеточном мозге и концентрации K + в плазме. Таким образом, изменение уровня K + мозга может иметь ключевое влияние на нейронную активность и сетевую активность во время и после гипераммониемии.Необходимы дополнительные исследования, чтобы изучить детали механизмов, участвующих в транспортировке аммиака через канал K + , чтобы изучить детали мозга.
Na
+ / K + / 2Cl — Сопутствующий транспортер (NKCC) Базолатерально или апикально локализованный ко-транспортер Na + / K + / 2Cl — (NKCC) транспортирует Na + , K + и 2Cl — электронейтрально. Две изоформы NKCC (1 и 2) были идентифицированы в нескольких клетках и тканях. У млекопитающих NKCC1 находится во многих типах клеток, таких как астроциты и нейроны, тогда как NKCC2 представлен в основном в почках.
Две изоформы NKCC (1 и 2) были идентифицированы в нескольких клетках и тканях. У млекопитающих NKCC1 находится во многих типах клеток, таких как астроциты и нейроны, тогда как NKCC2 представлен в основном в почках.
Недавние исследования показали, что NKCC1 в ткани мозга млекопитающих и в культурах клеток мозга принимают Nh5 + в качестве субстрата, субтитровав K + , что демонстрирует важность NKCC в системе транспорта аммиака в астроцитах. Было показано, что NKCC1 транспортирует Nh5 + в изолированные астроциты (Jayakumar et al., 2008). Недавние исследования также показали, что в культивируемых астроцитах крыс NKCC1 активировался в ответ на воздействие Nh5 +. Таким образом, увеличение активации NKCC было связано с набуханием астроцитов, процессом, который блокируется ингибитором NKCC (Jayakumar et al., 2008; Rangroo Thrane et al., 2013). Эти исследования подчеркивают роль NKCC в гомеостазе аммиака и набухании астроцитов.
Необходимость сравнительных исследований и перенос азота
В целом, нарушение регуляции системы транспорта азота из-за токсичности аммиака и любых изменений в экспрессии и функции переносчика аммиака может повлиять на гомеостаз и функцию аммиака в головном мозге, что может привести к серьезному повреждению нейронов в головном мозге с БА. Как упоминалось выше, изменения в экспрессии переносчиков аммиака, скорее всего, играют решающую роль в гомеостазе аммиака и набухании клеток; однако возможная связь между измененной функцией транспортера аммиака и AD все еще отсутствует. Следовательно, потребуются дополнительные исследования, чтобы изучить детали механизмов, участвующих в транспорте токсичного аммиака в нормальном мозге по сравнению с AD. Выяснение клинических патологических механизмов, связанных с транспортной системой аммиака, может дать общие ссылки на этиологию БА.В совокупности эти идеи имеют решающее значение для разработки терапевтических препаратов для изменения опасного притока аммиака, который вызывает повышенные системные уровни аммиака и, в конечном итоге, летальное повреждение мозга при БА.
Как упоминалось выше, изменения в экспрессии переносчиков аммиака, скорее всего, играют решающую роль в гомеостазе аммиака и набухании клеток; однако возможная связь между измененной функцией транспортера аммиака и AD все еще отсутствует. Следовательно, потребуются дополнительные исследования, чтобы изучить детали механизмов, участвующих в транспорте токсичного аммиака в нормальном мозге по сравнению с AD. Выяснение клинических патологических механизмов, связанных с транспортной системой аммиака, может дать общие ссылки на этиологию БА.В совокупности эти идеи имеют решающее значение для разработки терапевтических препаратов для изменения опасного притока аммиака, который вызывает повышенные системные уровни аммиака и, в конечном итоге, летальное повреждение мозга при БА.
Болезнь Альцгеймера (AD)
В настоящее время AD является наиболее распространенным прогрессирующим нейродегенеративным заболеванием в мире (Sperling et al., 2011). Клинически он характеризуется нарушением синаптической пластичности, обучения, памяти и некоторых других когнитивных функций (Albert, 1996). Нейропатологически БА характеризуется развитием внутриклеточных нейрофибриллярных клубков (NFT), образованных из состава гиперфосфорилированного тау-белка и скоплений внеклеточных сенильных бляшек (SP), которые собираются в результате отложения амилоида-β (Aβ) (Price and Morris, 1999; Sperling et al., 2011). Другой гистологический признак заболевания — неблагоприятный метаболизм белка-предшественника амилоида-β (AβPP) в SP и последующее накопление AβPP в поврежденных аксонах. Сверхэкспрессия AβPP генерирует каскад событий, которые включают гиперфосфорилированный тау, что приводит к синаптической недостаточности (Ward et al., 2012).
Помимо гиперфосфорилирования тау (Grundke-Iqbal et al., 1986) и отложения Aβ (Hardy and Selkoe, 2002), другие патологические аберрации включают: нарушение регуляции транскрипции (Pastorcic and Das, 2007), модифицированный нейровоспалительный процесс (Granic et al., 2009) и астроглиоз (Akude et al., 2011). Этиология и нейропатогенез БА позволяют предположить, что это заболевание является сложным и его лучше рассматривать как многофакторное нейродегенеративное заболевание с участием различных белков (Carreiras et al. , 2013). Что касается причинных факторов БА, были предложены различные гипотезы, включая нарушение энергетического метаболизма, дисфункцию митохондрий (Hoyer, 1998), изменения в системах рецепторов нейромедиаторов (таких как ГАМК, глутамат, МАО; Sims et al., 1998; Jones, 2002), дефицит микро-РНК (Nixon, 2013), повторный вход в клеточный цикл (Bonda et al., 2010), холинергический дефицит (Pinto et al., 2011), нейроиммуномодуляция (Akude et al., 2011) и дефицит гомеостаза кальция (Berridge, 2010) и многие другие.
, 2013). Что касается причинных факторов БА, были предложены различные гипотезы, включая нарушение энергетического метаболизма, дисфункцию митохондрий (Hoyer, 1998), изменения в системах рецепторов нейромедиаторов (таких как ГАМК, глутамат, МАО; Sims et al., 1998; Jones, 2002), дефицит микро-РНК (Nixon, 2013), повторный вход в клеточный цикл (Bonda et al., 2010), холинергический дефицит (Pinto et al., 2011), нейроиммуномодуляция (Akude et al., 2011) и дефицит гомеостаза кальция (Berridge, 2010) и многие другие.
Среди нейротоксических агентов, которые были изучены в отношении патологии БА, эффекту аммиака как сильнодействующего нейротоксина уделялось меньше внимания, чем оно того заслуживает. В этом обзоре упоминается несколько гипотез относительно этиологии аммиака при БА, включая недостаточность метаболизма глюкозы, митохондриальную дисфункцию, нарушение перенасыщения аматергической и ГАМКергической нейротрансмиссией, нарушение регуляции воспалительных реакций и дисфункцию памяти.
Нарушение энергетического метаболизма и митохондрии при БА и состояниях гипераммонии
Глюкоза является основным источником энергии в головном мозге, и нарушение метаболизма глюкозы имеет критические патофизиологические последствия. Несколько исследований указывают на значительное снижение гликолитического процесса в мозге с деменцией (Meier-Ruge et al., 1994; Simpson et al., 1994; Hoyer, 2000, 2004). Нарушение регуляции метаболизма глюкозы было продемонстрировано путем сравнения ферментативной активности переносчиков глюкозы (Simpson and Davies, 1994), гексокиназы (Marcus and Freedman, 1997), пируватдегидрогеназы (PDH) (Bubber et al., 2005) и ферменты цикла трикарбоновых кислот (TCA) при БА по сравнению с контрольными индивидуумами (Косенко и др., 2014).
Высокие концентрации аммиака приводят к повышенному содержанию астроцитарного глутамина с уменьшением концентрации глутамата, что вызывает снижение активности малат-аспаратного челнока (MAS). В результате нарушения МАС соотношение пируват / лактат в астроцитах снижается. Не связанные с активностью MAS, высокие концентрации аммиака как в астроцитах, так и в нейронах могут ингибировать декарбоксилирование альфа-кетоглутарата в цикле TCA, что приводит к ингибированию PDH (Hertz and Kala, 2007).
Не связанные с активностью MAS, высокие концентрации аммиака как в астроцитах, так и в нейронах могут ингибировать декарбоксилирование альфа-кетоглутарата в цикле TCA, что приводит к ингибированию PDH (Hertz and Kala, 2007).
Помимо недостаточности метаболизма глюкозы, в мозге при БА нарушается функциональность митохондрий. Это включает: увеличение производства активных форм кислорода (АФК), нарушение баланса между делением и слиянием митохондрий, изменения морфологии митохондрий, ферментативную недостаточность митохондрий и снижение скорости митохондриального аксонального транспорта (Рисунок 2; Zhu et al., 2013 ; Cadonic et al., 2015).
Хотя была выдвинута гипотеза, что регуляция митохондрий обычно генетически врожденная, на активность митохондрий могут влиять другие нейротоксические факторы, такие как аммиак.Несколько исследований показывают, что аммиак ставит под угрозу различные части биоэнергетического аппарата клетки. Например, активность нескольких ферментов ETC, митохондриальной цитохром с оксидазы, глутатионпероксидазы и супероксидазы дисмутазы значительно снижается в мозге, обработанном аммиаком (Kosenko et al. , 1997, 1999, 2004, 2007; Qureshi et al., 1998; Esteves et al., 2009). Кроме того, активность супероксидазы, АФК и поли (АДФ-рибоза) полимеразы (PARP) увеличивалась в митохондриях мозга при стрессовом состоянии, вызванном анаммонией (Kosenko et al., 2003, 2004; Морейра и др., 2008). Существующие данные указывают на то, что энергетический метаболизм нарушается при AD, а аммиак участвует в нарушении энергетического обмена (т.е. митохондриальной дисфункции) при AD. Однако необходимы дополнительные исследования, чтобы лучше понять, как митохондрии подвержены влиянию высоких концентраций аммиака, как AD по сравнению с нормальными клетками мозга млекопитающих справляются с дефицитом энергии и как эти органеллы защищают себя от массивного притока токсичного аммиака в мозг.
Влияние аммиака на возбуждающую глутаматергическую и ГАМКергическую нейротрансмиссию
Одна из важнейших функций астроцитов — защищать нейроны от эксайтотоксичности, поглощая избыток аммиака (NH 3 ) и глутамата (Glu) и превращая его в глутамин (Gln) через аденозинтрифосфат-зависимую глутаминсинтазу (GS). В печени и нейронах Gln гидролизуется через фосфат-зависимую глутаминазу до Glu и аммиака (NH 3 ) (Zielke et al., 1989; Smith, 1990).
Было показано, что у людей с HE отсутствует баланс между возбуждающей и тормозной нейротрансмиссией. Основное ингибирование происходит из-за снижения экспрессии рецепторов Glu, что приводит к снижению глутаматергического тонуса. Более того, ингибирование транспортеров глутамата (Glt-1) у пациентов с HE приводит к снижению повторного захвата Glu астроцитами после чрезмерного внесинаптического накопления Glu (Albrecht and Jones, 1999).
Более того, аномальный метаболизм аммиака в мозге при БА коррелирует со снижением активности GS астроцитов (Suarez et al., 2002). Изменения уровня экспрессии GS при стрессовом состоянии, вызванном аммиаком, могут изменять морфологию астроглии (астроцитоз), что может отражаться на функции нейронов (рис. 2). Изменения в регуляции GS предполагают, что цикл Glu-Gln может дифференциально нарушаться при AD. Кроме того, более низкая активность GS связана с плотностью внеклеточных отложений Aβ и SP в коре головного мозга при БА (Le Prince et al., 1995). Было продемонстрировано, что Aβ может взаимодействовать с GS и вызывать окислительную инактивацию этого фермента, а также усиливать нейротоксичность Aβ.В соответствии с этими данными предполагается, что существует связь между нарушенной детоксикацией аммиака (из-за изменения активности GS) и образованием амилоидных бляшек в мозге при БА (Аксенов и др., 1997; Робинсон, 2000).
Кроме того, более низкая активность GS связана с плотностью внеклеточных отложений Aβ и SP в коре головного мозга при БА (Le Prince et al., 1995). Было продемонстрировано, что Aβ может взаимодействовать с GS и вызывать окислительную инактивацию этого фермента, а также усиливать нейротоксичность Aβ.В соответствии с этими данными предполагается, что существует связь между нарушенной детоксикацией аммиака (из-за изменения активности GS) и образованием амилоидных бляшек в мозге при БА (Аксенов и др., 1997; Робинсон, 2000).
Помимо влияния аммиака на глутаматергический тонус, аммиак также может изменять систему гамма-аминомасляной кислоты (ГАМК) в головном мозге. ГАМК является одним из факторов, опосредующих тормозную нейротрансмиссию. Например, чрезмерные уровни аммиака увеличивают высвобождение ГАМК, что приводит к усилению ГАМКергической системы при БА.Таким образом, дисбаланс нейротрансмиссии, вызванный аммиаком, может быть ответственным за когнитивный дефицит при БА (Seiler, 2002; Rama Rao et al. , 2010). Однако механизмы, с помощью которых аммиак способствует проявлению БА, остаются плохо определенными.
, 2010). Однако механизмы, с помощью которых аммиак способствует проявлению БА, остаются плохо определенными.
Воспалительные реакции, вызванные аммиаком, в
г. н.э. Повышенный уровень аммиака в головном мозге способен влиять на важные воспалительные процессы, вызывая изменения высвобождения цитокинов и воспалительных белков микроглией, астроглиомой, астроцитами и нейронами (рис. 2).Кроме того, повышенные уровни аммиака вызывают апоптоз, который связан с дегенерацией нейронов, посредством различных сигнальных молекул, таких как ядерный фактор-каппа B (NF-κB) (Buzanska et al., 2000). NF-kB является фактором транскрипции, играющим критическую роль в регуляции воспалительных реакций, врожденного иммунитета, апопотоза и митохондриальной дисфункции (Barnes and Adcock, 1997; Henderson et al., 2002; Sinke et al., 2008; Shi et al. ., 2014). К ним относятся индуцибельная синтаза оксида азота (iNOS), оксид азота (NO), NADPH-оксидаза (NOX), супероксид и пероксинитрит, фосфолипаза A2 (PLA2) и цикооксигеназа-2 (COX-2), которые, как было доказано, способны индуцировать астроциты. припухлость.Недавние исследования также показали, что аммиак активирует iNOS, NOX, PLA2 и COX-2, а ингибирование вышеупомянутых ферментов значительно уменьшает набухание астроцитов, вызванное аммиаком. Кроме того, иммуногистохимический анализ показал, что обработанные аммиаком культуры астроцитов способны увеличивать активность NF-κB и набухание астроцитов. Блокирование активности NF-κB с помощью BAY 11-7082 приводит к снижению вызванного аммиаком набухания в культивируемых астроцитах (Sinke et al., 2008; Rama Rao et al., 2010; Rao et al., 2010). Эти данные указывают на критическую роль аммиака в активации NF-κB и, в конечном итоге, в набухании астроцитов. Однако механизмы, которые лежат в основе того, как сигнальные пути NF-κB способствуют набуханию астроцитов, полностью не изучены. Такое непонимание открывает потенциальные возможности для дальнейших исследований.
припухлость.Недавние исследования также показали, что аммиак активирует iNOS, NOX, PLA2 и COX-2, а ингибирование вышеупомянутых ферментов значительно уменьшает набухание астроцитов, вызванное аммиаком. Кроме того, иммуногистохимический анализ показал, что обработанные аммиаком культуры астроцитов способны увеличивать активность NF-κB и набухание астроцитов. Блокирование активности NF-κB с помощью BAY 11-7082 приводит к снижению вызванного аммиаком набухания в культивируемых астроцитах (Sinke et al., 2008; Rama Rao et al., 2010; Rao et al., 2010). Эти данные указывают на критическую роль аммиака в активации NF-κB и, в конечном итоге, в набухании астроцитов. Однако механизмы, которые лежат в основе того, как сигнальные пути NF-κB способствуют набуханию астроцитов, полностью не изучены. Такое непонимание открывает потенциальные возможности для дальнейших исследований.
Данные указывают на то, что активация воспалительных реакций является патологическим признаком БА. Нейровоспаление при БА характеризуется повышенной активностью воспалительных цитокинов, таких как IL-6, IL-1β и TNF-α. Поскольку нейровоспаление является одним из ключевых факторов как БА, так и состояния гипераммонии, предполагается, что нацеливание на нейровоспалительные медиаторы, такие как NF-κB, может обеспечить эффективную стратегию лечения неврологических нарушений, связанных с повышенным уровнем аммиака.
Поскольку нейровоспаление является одним из ключевых факторов как БА, так и состояния гипераммонии, предполагается, что нацеливание на нейровоспалительные медиаторы, такие как NF-κB, может обеспечить эффективную стратегию лечения неврологических нарушений, связанных с повышенным уровнем аммиака.
Аммиак и память
Нарушение памяти — один из основных нейропатологических признаков БА (Albert, 1996). Повышение концентрации аммиака постепенно приводит к нарушению психического статуса (когнитивное, пространственное обучение и дисфункции памяти).В 2000 году Агилар и др. показали, что воздействие высоких концентраций аммиака на срезы гиппокампа крыс нарушает рецепторы NMDA, что впоследствии ухудшает память или условное обучение у животных (Aguilar et al., 2000). Другие возможные механизмы дефицита обучения, вызванного высокими уровнями аммиака, скорее всего, связаны с сокращением нейронального пути глутамат-оксид азота (NO) -циклический GMP. Интересно, что снижение образования NO коррелировало с интеллектуальной дисфункцией у пациентов с деменцией при БА, но не у пациентов с сосудистой деменцией (Косенко и др. , 2014).
, 2014).
Кроме того, было высказано предположение, что хроническое воздействие аммиака влияет на когнитивные функции через метаболизм нейростероидов. Аммиак нарушает синтез нейростероидов, что, как полагают, участвует в ухудшении памяти. Также было показано, что аммиак нарушает долгосрочную потенциацию (ДП) в гиппокампе, и этот механизм считается критически важным для формирования памяти. В конечном итоге аммиак может модулировать метаболизм нейростероидов за счет чрезмерной активации рецепторов NMDA и ингибирования LTP за счет эффекта, опосредованного рецепторами ГАМК (Izumi et al., 2013).
Заключение
Прошло чуть более 20 лет с тех пор, как была опубликована первая гипотеза, предполагающая, что существует связь между аммиаком и БА (Seiler, 1993). С тех пор было проведено очень мало прямых исследований в пользу патофизиологической роли аммиака в головном мозге при БА. Однако, поскольку высокие концентрации аммиака в головном мозге были обнаружены при AD, характеристика физиологических и молекулярных механизмов системы транспорта аммиака в клетках мозга при AD по сравнению с контролем теперь даст лучшее понимание того, изменяется ли транспорт аммиака при AD. Получение знаний о механизмах транспорта азота и его регуляции при БА будет иметь прямое отношение к области медицины.
Хотя аммиак вряд ли является основной причиной БА, он действует как мощный нейротоксин, влияя на различные биологические пути, такие как нарушение энергетического обмена, дисфункция митохондрий, нарушение регуляции воспалительной реакции и дисфункция памяти. Интересно, что эти пути также способствуют возникновению и / или прогрессированию AD. Вышеупомянутые факторы также наблюдались при AD.Таким образом, необходимы дополнительные исследования для изучения потенциальной связи между токсичностью аммиака и БА. Полагают, что исследование этой потенциальной связи в значительной степени поможет в разработке терапевтических препаратов для изменения опасного притока аммиака в мозг при БА и предотвращения летального повреждения клеток мозга при БА.
Авторские взносы
AA: сформулировал исследование и написал рукопись. МС: рассчитанные цифры. БА: представил интеллектуальные мысли, отредактировал рукопись и руководитель проекта.
Финансирование
Эта работа финансировалась грантами Исследовательского общества Манитобы / Альцгеймера и Фонда исследований больницы Св. Бонифация [номера грантов: 1406-3216, 1403-3131 и 1410-3216].
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Список литературы
Adlimoghaddam, A., Boeckstaens, M., Марини, А. М., Треберг, Дж. Р., Брассинга, А. К., и Вейрах, Д. (2015). Экскреция аммиака в Caenorhabditis elegans : механизм и доказательства транспорта аммиака резус-белка CeRhr-1. J Exp Biol. 218 (Pt 5), 675–683. DOI: 10.1242 / jeb.111856
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Adlimoghaddam, A., O’Donnell, M.J., Kormish, J., Banh, S., Treberg, J.R., Merz, D., et al. (2016). Экскреция аммиака в Caenorhabditis elegans : физиологическая и молекулярная характеристика нокаутированного мутанта rhr-2. Сост. Биохим. Physiol. Мол. Интегр. Physiol. 195, 46–54. DOI: 10.1016 / j.cbpa.2016.02.003
Сост. Биохим. Physiol. Мол. Интегр. Physiol. 195, 46–54. DOI: 10.1016 / j.cbpa.2016.02.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Агилар, М.А., Минарро, Дж., И Фелипо, В. (2000). Хроническая умеренная гипераммонемия нарушает активное и пассивное поведение избегания и условную дискриминацию у крыс. Exp. Neurol. 161, 704–713. DOI: 10.1006 / exnr.1999.7299
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Аксенов, М.Ю., Аксенова, М. В., Карни, Дж. М., и Баттерфилд, Д. А. (1997). Окислительная модификация глутамин синтетазы бета-амилоидным пептидом. Free Radic. Res. 27, 267–281. DOI: 10.3109 / 107157697065
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Акуде, Э., Жеребицкая, Э., Чоудхури, С. К., Смит, Д. Р., Добровский, Р. Т., и Фернихо, П. (2011). Уменьшение образования супероксида связано с дисфункцией дыхательной цепи и изменениями в митохондриальном протеоме сенсорных нейронов крыс с диабетом. Диабет 60, 288–297. DOI: 10.2337 / db10-0818
Диабет 60, 288–297. DOI: 10.2337 / db10-0818
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Альбрехт Дж., Хильджер В. и Вальски М. (1994). Аммиак добавил in vitro , но не умеренную гипераммониемию in vivo , стимулирует поглощение глутамата и активность H + -АТФазы в синаптических пузырьках головного мозга крысы. Metab. Brain Dis. 9, 257–266. DOI: 10.1007 / BF019
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Альбрехт, Дж., и Джонс, Э.А. (1999). Печеночная энцефалопатия: молекулярные механизмы, лежащие в основе клинического синдрома. J. Neurol. Sci. 170, 138–146. DOI: 10.1016 / S0022-510X (99) 00169-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Атанасов, К. Л., Мюллер, К. Д., Дюмон, С., Ребел, Г., Пуиндрон, П., и Зайлер, Н. (1995). Влияние аммиака на эндоцитоз и продукцию цитокинов иммортализованными клетками микроглии и астроглии человека. Neurochem. Int. 27, 417–424.DOI: 10.1016 / 0197-0186 (95) 00023-2
Int. 27, 417–424.DOI: 10.1016 / 0197-0186 (95) 00023-2
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Атанасов, К. Л., Мюллер, К. Д., Сархан, С., Кнодген, Б., Ребел, Г., и Зайлер, Н. (1994). Влияние аммиака на эндоцитоз, продукцию цитокинов и активность лизосомальных ферментов линии клеток микроглии. Res. Иммунол. 145, 277–288. DOI: 10.1016 / S0923-2494 (94) 80016-2
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бенджеллун, Ф., Бакух, Н., Fritsch, J., Hulin, P., Lipecka, J., Edelman, A., et al. (2005). Экспрессия гликопротеина Rh эритроида человека (RhAG) усиливает транспорт как Nh4, так и Nh5 + в клетках HeLa. Pflugers Arch. 450, 155–167. DOI: 10.1007 / s00424-005-1381-y
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бонда, Д. Дж., Ван, X., Перри, Г., Нуномура, А., Табатон, М., Чжу, X., et al. (2010). Окислительный стресс при болезни Альцгеймера: возможность профилактики. Нейрофармакология 59, 290–294.DOI: 10.1016 / j.neuropharm.2010.04.005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бритто, Д. Т., и Кронзакер, Х. Дж. (2002). Токсичность Nh5 + для высших растений: критический обзор. J. Plant Physiol. 159, 567–584. DOI: 10.1078 / 0176-1617-0774
CrossRef Полный текст | Google Scholar
Буббер П., Арутюнян В., Фиш Г., Бласс Дж. П. и Гибсон Г. Э. (2005). Митохондриальные аномалии в мозге при болезни Альцгеймера: механистические последствия. Ann. Neurol. 57, 695–703. DOI: 10.1002 / ana.20474
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бузанска, Л., Заблока, Б., Дыбель, А., Доманска-Яник, К., и Альбрехт, Дж. (2000). Задержка индукции апоптоза аммиаком в клетках глиомы C6. Neurochem. Int. 37, 287–297. DOI: 10.1016 / S0197-0186 (00) 00030-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Cadonic, C., Sabbir, M. G., and Albensi, B.C.(2015). Механизмы митохондриальной дисфункции при болезни Альцгеймера. Мол. Neurobiol. DOI: 10.1007 / s12035-015-9515-5. [Epub перед печатью].
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кэмерон, Дж. Н. и Хейслер, Н. (1983). Исследования аммиака в радужной форели: физико-химические параметры, кислотно-щелочное поведение и респираторный клиренс. J. Exp. Биол. 105, 107–125.
Google Scholar
Каррейрас, М. К., Мендес, Э., Перри, М. Дж., Франциско, А. П., и Марко-Контеллес, Дж. (2013). Многофакторный характер болезни Альцгеймера для разработки потенциальных терапевтических средств. Curr. Вершина. Med. Chem. 13, 1745–1770. DOI: 10.2174 / 156802661131399
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чан, Х., Хазелл, А.С., Дежарден, П., и Баттерворт, Р.Ф. (2000). Влияние аммиака на белок переносчика глутамата (GLAST) и мРНК в культивируемых кортикальных астроцитах крыс. Neurochem. Int. 37, 243–248. DOI: 10.1016 / S0197-0186 (00) 00026-7
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чан, С.Х., Лей, В.Дж., Сюй, Л.С., Чанг, Х.С., Хван, Т.Л., Чен, И.С. и др. (2013). Ривезиозид F индуцирует мощную и эффективную антипролиферативную и апоптотическую активность через митохондриальный стресс, связанный с субъединицей Na (+) / K (+) — АТФазы альфа3, и усиление каспазных каскадов. Biochem. Pharmacol. 86, 1564–1575.DOI: 10.1016 / j.bcp.2013.09.021
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Дай, Х., Сун, Д., Сюй, Дж., Ли, Б., Герц, Л., и Пэн, Л. (2013). Индуцированная аммиаком трансактивация рецептора EGF, опосредованная Na, K-АТФазой / уабаином, передача сигналов MAPK / ERK и PI3K / AKT и образование ROS вызывают набухание астроцитов. Neurochem. Int. 63, 610–625. DOI: 10.1016 / j.neuint.2013.09.005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Эриксон Р.Дж. (1985). Оценка математических моделей влияния pH и температуры на токсичность аммиака для водных организмов. Water Res. 19, 1047–1058. DOI: 10.1016 / 0043-1354 (85) -6
CrossRef Полный текст | Google Scholar
Эстевес, А. Р., Ардуино, Д. М., Свердлов, Р. Х., Оливейра, К. Р., и Кардосо, С. М. (2009). Участие окислительного стресса в олигомеризации альфа-синуклеина у цибридов болезни Паркинсона. Антиоксид. Редокс-сигнал. 11, 439–448.DOI: 10.1089 / ARS.2008.2247
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гранич И., Долга А. М., Нейхольт И. М., ван Дейк Г. и Эйзель У. Л. (2009). Воспаление и NF-kappaB при болезни Альцгеймера и диабете. J. Alzheimers. Дис. 16, 809–821. DOI: 10.3233 / JAD-2009-0976
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Грегориос, Дж. Б., Мозес, Л. В., Норенберг, Л. О., и Норенберг, М. Д. (1985). Морфологические эффекты аммиака на первичные культуры астроцитов.I. Световые микроскопические исследования. J. Neuropathol. Exp. Neurol. 44, 397–403. DOI: 10.1097 / 00005072-198507000-00003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Grundke-Iqbal, I., Iqbal, K., Tung, Y.C., Quinlan, M., Wisniewski, H.M, and Binder, L.I. (1986). Аномальное фосфорилирование тау-белка, связанного с микротрубочками (тау), при патологии цитоскелета, вызванной болезнью Альцгеймера. Proc. Natl. Акад. Sci. США 83, 4913–4917. DOI: 10.1073 / pnas.83.13.4913
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Грусвиц, Ф., Чаудхари, С., Хо, Дж. Д., Шлессингер, А., Пезешки, Б., Хо, К. М. и др. (2010). Функция Rh человека на основе структуры RhCG при 2,1 A. Proc. Natl. Акад. Sci. США 107, 9638–9643. DOI: 10.1073 / pnas.1003587107
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хамм, Л. Л., и Саймон, Э. Э. (1990). Транспорт аммиака в проксимальном канальце. Шахтер.Электролит Метаб. 16, 283–290.
PubMed Аннотация | Google Scholar
Харди Дж. И Селкое Д. Дж. (2002). Амилоидная гипотеза болезни Альцгеймера: прогресс и проблемы на пути к терапии. Наука 297, 353–356. DOI: 10.1126 / science.1072994
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хендерсон, К. К., Вагнер, Х., Фаврет, Ф., Бриттон, С. Л., Кох, Л. Г., Вагнер, П. Д. и др. (2002). Детерминанты максимального поглощения O (2) у крыс, селективно разводимых на выносливость при беге. J. Appl. Physiol. (1985). 93, 1265–1274. DOI: 10.1152 / japplphysiol.00809.2001
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Герц, Л., Пэн, Л., и Сонг, Д. (2015). Аммиак, как и K (+), стимулирует Na (+), K (+), 2 Cl (-) котранспортер NKCC1 и Na (+), K (+) — АТФазу и взаимодействует с эндогенным уабаином в астроцитах. Neurochem. Res. 40, 241–257. DOI: 10.1007 / s11064-014-1352-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хойер, С.(1998). Является ли спорадическая болезнь Альцгеймера типом мозга инсулинозависимого сахарного диабета? Сложная гипотеза. J. Neural. Трансм (Вена). 105, 415–422. DOI: 10.1007 / s007020050067
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хойер, С. (2000). Нарушения глюкозы в головном мозге и энергетического обмена при спорадической болезни Альцгеймера. Причины и последствия: обновление. Exp. Геронтол. 35, 1363–1372. DOI: 10.1016 / S0531-5565 (00) 00156-X
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хойер, С.(2004). Причины и последствия нарушений церебрального метаболизма глюкозы при спорадической болезни Альцгеймера: терапевтические последствия. Adv. Exp. Med. Биол. 541, 135–152. DOI: 10.1007 / 978-1-4419-8969-7_8
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хойер, С., Остеррайх, К., и Вагнер, О. (1988). Метаболизм глюкозы как место первичной аномалии при раннем начале деменции типа Альцгеймера? J. Neurol. 235, 143–148. DOI: 10.1007 / BF00314304
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Hrnjez, B. J., Song, J. C., Prasad, M., Mayol, J. M., and Matthews, J. B. (1999). Аммиачная блокада кишечного эпителия K + проводимость. Am. J. Physiol. 277 (3, часть 1), G521 – G532.
PubMed Аннотация | Google Scholar
Ху, Ю. К., и Каплан, Дж. Х. (2000). Сайт-направленное химическое мечение внеклеточных петель в мембранном белке. Топология альфа-субъединицы Na, K-АТФазы. J. Biol. Chem. 275, 19185–19191. DOI: 10.1074 / jbc.M000641200
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хуанг, К. Х., и Пэн, Дж. (2005). Эволюционная консервация и диверсификация генов и белков семейства Rh. Proc. Natl. Акад. Sci. США 102, 15512–15517. DOI: 10.1073 / pnas.0507886102
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хуанг, Х., Винтер, Э. Э., Ван, Х., Вайншток, К. Г., Xing, H., Goodstadt, L., et al. (2004). Эволюционная консервация и отбор ортологов генов болезней человека в геномах крыс и мышей. Genome Biol. 5: R47. DOI: 10.1186 / GB-2004-5-7-r47
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Идзуми Ю., Свракич Н., О’Делл К. и Зорумски К. Ф. (2013). Аммиак подавляет долгосрочное потенцирование за счет синтеза нейростероидов в пирамидных нейронах гиппокампа. Неврология 233, 166–173. DOI: 10.1016 / j.neuroscience.2012.12.035
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джаякумар А. Р., Лю М., Морияма М., Рамакришнан Р., Форбуш Б. III, Редди П. В. и др. (2008). Na-K-Cl Котранспортер-1 в механизме индуцированного аммиаком набухания астроцитов. J. Biol. Chem. 283, 33874–33882. DOI: 10.1074 / jbc.M804016200
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кнехт, К., Михалак, А., Роуз, К., Ротштейн, Дж.Д. и Баттерворт Р. Ф. (1997). Снижение экспрессии транспортера глутамата (GLT-1) в лобной коре головного мозга крыс с острой печеночной недостаточностью. Neurosci. Lett. 229, 201–203. DOI: 10.1016 / S0304-3940 (97) 00444-8
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Неппер М.А., Пакер Р. и Гуд Д. У. (1989). Транспорт аммония в почках. Physiol. Ред. 69, 179–249.
PubMed Аннотация | Google Scholar
Косенко, Е.А., Соломадин, И. Н., Тихонова, Л. А., Редди, В. П., Алиев, Г., Каминский, Ю. Г. (2014). Патогенез болезни Альцгеймера: роль окислительного стресса, бета-амилоидных пептидов, системный аммиак и энергетический обмен эритроцитов. CNS Neurol. Disord. Цели наркотиков. 13, 112–119. DOI: 10.2174 / 18715273113126660130
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Косенко Е. А., Венедиктова Н. И., Каминский Ю. Г. (2003). [Кальций и аммиак стимулируют активность моноаминоксидазы А в митохондриях мозга]. Изв. Акад. Наук сер. Биол. 30, 449–452. DOI: 10.1023 / A: 1025834232678
CrossRef Полный текст | Google Scholar
Косенко, Э., Фелипо, В., Монтолиу, К., Гризолия, С., Каминский, Ю. (1997). Эффекты острой гипераммониемии in vivo на окислительный метаболизм в несинаптических митохондриях головного мозга крыс. Metab. Brain Dis. 12, 69–82. DOI: 10.1007 / BF02676355
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Косенко, Е., Камински Ю., Лопата О., Муравьев Н. и Фелипо В. (1999). Блокирование рецепторов NMDA предотвращает окислительный стресс, вызванный острой интоксикацией аммиаком. Free Radic. Биол. Med. 26, 1369–1374. DOI: 10.1016 / S0891-5849 (98) 00339-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Косенко Е., Каминский Ю., Соломадин И., Маров Н., Венедиктова Н., Фелипо В. и др. (2007). Острая нейротоксичность аммиака in vivo включает увеличение цитоплазматического белка Р53 без изменений других маркеров апоптоза. J. Neurosci. Res. 85, 2491–2499. DOI: 10.1002 / jnr.21385
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Косенко Е., Монтолиу К., Джордано Г., Каминский Ю., Венедиктова Н., Бурьянов Ю. и др. (2004). Острая аммиачная интоксикация вызывает опосредованное рецептором NMDA повышение уровня поли (АДФ-рибозы) полимеразы и метаболизма НАД в ядрах клеток головного мозга крысы. J. Neurochem. 89, 1101–1110. DOI: 10.1111 / j.1471-4159.2004.02426.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ларсен, Э.Х., Дитон, Л. Е., Онкен, Х., О’Доннелл, М., Грозелл, М., Данцлер, В. Х. и др. (2014). Осморегуляция и выведение. Компр. Physiol. 4, 405–573. DOI: 10.1002 / cphy.c130004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лаурсен, Х., Димер, Н. Х. (1979). Морфометрические исследования ультраструктуры глиальных клеток крыс после гипераммонемии, вызванной уреазой. Neuropathol. Прил. Neurobiol. 5, 345–362. DOI: 10.1111 / j.1365-2990.1979.tb00634.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лемберг, А., и Фернандес, М.А. (2009). Печеночная энцефалопатия, аммиак, глутамат, глутамин и окислительный стресс. Ann. Гепатол. 8, 95–102.
PubMed Аннотация | Google Scholar
Ле Принс, Г., Делар, П., Фаж, К., Лефрансуа, Т., Турэ, М., Саланон, М., и др. (1995). Экспрессия глутамин синтетазы (GS) снижается при старческом слабоумие типа Альцгеймера. Neurochem. Res. 20, 859–862. DOI: 10.1007 / BF00969698
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Lichter-Konecki, U., Мангин, Дж. М., Гордиш-Дрессман, Х., Хоффман, Э. П. и Галло, В. (2008). Профили экспрессии генов астроцитов от гипераммониемных мышей выявляют измененные пути гомеостаза воды и калия in vivo . Glia 56, 365–377. DOI: 10.1002 / glia.20624
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Liu, Z., Chen, Y., Mo, R., Hui, C., Cheng, J.F., Mohandas, N., et al. (2000). Характеристика RhCG человека и Rhcg мыши как новых неэритроидных гомологов гликопротеина Rh, преимущественно экспрессируемых в почках и семенниках. J. Biol. Chem. 275, 25641–25651. DOI: 10.1074 / jbc.M003353200
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Маркаджи П. и Коулз Дж. А. (2001). Аммоний в нервной ткани: транспорт через клеточные мембраны, потоки от нейронов к глиальным клеткам и роль в передаче сигналов. Прог. Neurobiol. 64, 157–183. DOI: 10.1016 / S0301-0082 (00) 00043-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Marcaida, G., Felipo, V., Hermenegildo, C., Minana, M. D., and Grisolia, S. (1992). Острая токсичность аммиака опосредуется глутаматными рецепторами типа NMDA. FEBS Lett. 296, 67–68. DOI: 10.1016 / 0014-5793 (92) 80404-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Маркус, Д. Л., и Фридман, М. Л. (1997). Снижение метаболизма глюкозы в мозге в микрососудах у пациентов с болезнью Альцгеймера. Ann. N.Y. Acad. Sci. 826, 248–253. DOI: 10.1111 / j.1749-6632.1997.tb48476.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Марини, А. М., Матасси, Г., Райнал, В., Андре, Б., Картрон, Дж. П., и Шериф-Захар, Б. (2000). Связанный с резусом белок RhAG человека и его гомолог почек способствуют транспорту аммония в дрожжах. Nat. Genet. 26, 341–344. DOI: 10.1038 / 81656
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мейер-Руге, В., Бертони-Фреддари, К., и Ивангоф, П. (1994). Изменения метаболизма глюкозы в головном мозге как ключ к патогенезу болезни Альцгеймера. Геронтология 40, 246–252. DOI: 10.1159 / 000213592
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Морейра П. И., Нуномура А., Накамура М., Такеда А., Шенк Дж. К., Алиев Г. и др. (2008). Окисление нуклеиновых кислот при болезни Альцгеймера. Free Radic. Биол. Med. 44, 1493–1505. DOI: 10.1016 / j.freeradbiomed.2008.01.002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мурти, К. Р., Рама Рао, К. В., Бай, Г., и Норенберг, М. Д. (2001). Вызванное аммиаком производство свободных радикалов в первичных культурах астроцитов крыс. J. Neurosci. Res. 66, 282–288. DOI: 10.1002 / jnr.1222
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Муса-Азиз, Р., Чен, Л. М., Пеллетье, М. Ф., и Борон, В. Ф. (2009). Относительная селективность CO2 / Nh4 для AQP1, AQP4, AQP5, AmtB и RhAG. Proc. Natl. Акад. Sci. США 106, 5406–5411. DOI: 10.1073 / pnas.0813231106
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Накада, Т., Вестхофф, К. М., Като, А., и Хиросе, С. (2007). Секреция аммиака из жабр рыб зависит от набора гликопротеинов Rh. FASEB J. 21, 1067–1074. DOI: 10.1096 / fj.06-6834com
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Навата, К. М., Хунг, К. К., Цуй, Т. К., Уилсон, Дж. М., Райт, П. А. и Вуд, К. М. (2007). Экскреция аммиака у радужной форели (Oncorhynchus mykiss): доказательства участия гликопротеина Rh и H + -АТФазы. Physiol. Геномика 31, 463–474.DOI: 10.1152 / Physiolgenomics.00061.2007
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Навата, К. М., и Вуд, К. М. (2009). Анализ экспрессии мРНК физиологических ответов на вливание аммиака у радужной форели. J. Comp. Physiol. Б. 179, 799–810. DOI: 10.1007 / s00360-009-0361-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Норенберг М. Д., Хо З., Нари Дж. Т. и Роиг-Кантесано А. (1997). Глиальный транспортер глутамата при гипераммониемии и печеночной энцефалопатии: связь с энергетическим метаболизмом и глутаматергической нейротрансмиссией. Glia 21, 124–133.
PubMed Аннотация | Google Scholar
О’Доннелл, М. Дж. (1997). «Механизмы выделения и ионный транспорт у беспозвоночных», в Сравнительная физиология , изд. У. Х. Данцлер (Нью-Йорк, Нью-Йорк: Oxford University Press), 1207–1289.
Отт П. и Ларсен Ф. С. (2004). Проницаемость гематоэнцефалического барьера для аммиака при печеночной недостаточности: критическая переоценка. Neurochem. Int. 44, 185–198. DOI: 10.1016 / S0197-0186 (03) 00153-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Пасторчич, М., и Дас, Х. К. (2007). Анализ модуляции транскрипции промотора гена пресенилина 1 с помощью ZNF237, кандидата на связывание фактора транскрипции Ets ERM. Brain Res. 1128, 21–32. DOI: 10.1016 / j.brainres.2006.10.056
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Пинто, Т., Ланкто, К. Л., и Херрманн, Н. (2011). Пересмотр холинергической гипотезы поведенческих и психологических симптомов при деменции типа Альцгеймера. Aging Res.Ред. 10, 404–412. DOI: 10.1016 / j.arr.2011.01.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Пиццония, Дж. Х., Рэнсом, Б. Р. и Паппас, К. А. (1996). Характеристика активности обмена Na + / H + в культивируемых астроцитах гиппокампа крыс. J. Neurosci. Res. 44, 191–198.
PubMed Аннотация | Google Scholar
Прайс, Дж. Л., и Моррис, Дж. К. (1999). Клубки и бляшки при недемментированном старении и «доклинической» болезни Альцгеймера. Ann. Neurol. 45, 358–368.
PubMed Аннотация | Google Scholar
Куреши К., Рао К. В. и Куреши И. А. (1998). Дифференциальное ингибирование гипераммониемией ферментов цепи переноса электронов в синаптосомах и несинаптических митохондриях у spf-мышей с дефицитом орнитин-транскарбамилазы: восстановление ацетил-L-карнитином. Neurochem. Res. 23, 855–861. DOI: 10.1023 / A: 1022406
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Рама Рао, К.В., Джаякумар А. Р., Тонг X., Альварес В. М. и Норенберг М. Д. (2010). Заметное усиление набухания клеток цитокинами в культивируемых астроцитах, сенсибилизированных аммиаком. J. Нейровоспаление 7:66. DOI: 10.1186 / 1742-2094-7-66
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Рама Рао, К. В., Веркман, А. С., Кертис, К. М., и Норенберг, М. Д. (2014). Делеция аквапорина-4 у мышей снижает энцефалопатию и отек мозга при экспериментальной острой печеночной недостаточности. Neurobiol. Дис. 63, 222–228. DOI: 10.1016 / j.nbd.2013.11.018
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Рангру Трейн, В., Трейн, А.С., Ван, Ф., Котрина, М.Л., Смит, Н.А., Чен, М., и др. (2013). Аммиак вызывает растормаживание нейронов и судороги, нарушая буферизацию калия астроцитами. Nat. Med. 19, 1643–1648. DOI: 10,1038 / нм 3400
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Рао, К.В., Джаякумар, А. Р., Редди, П. В., Тонг, X., Кертис, К. М., и Норенберг, М. Д. (2010). Аквапорин-4 в культивированных астроцитах, обработанных марганцем. Glia 58, 1490–1499. DOI: 10.1002 / glia.21023
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Робинсон, С. Р. (2000). Экспрессия глутамин синтетазы в нейронах при болезни Альцгеймера указывает на глубокое нарушение метаболических взаимодействий с астроцитами. Neurochem. Int. 36, 471–482. DOI: 10.1016 / S0197-0186 (99) 00150-3
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ши К., Чжу X., Ван Дж. И Лонг Д. (2014). Интромитохондриальный сигнальный путь IkappaB / NF-kappaB участвует в митохондриальной дисфункции, индуцированной амилоидным бета-пептидом. J. Bioenerg. Биомембр. 46, 371–376. DOI: 10.1007 / s10863-014-9567-7
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Симпсон, И. А., Чунду, К. Р., Дэвис-Хилл, Т., Хонер, В. Г., и Дэвис, П. (1994). Снижение концентрации переносчиков глюкозы GLUT1 и GLUT3 в головном мозге пациентов с болезнью Альцгеймера. Ann. Neurol. 35, 546–551. DOI: 10.1002 / ana.410350507
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Симпсон, И. А., и Дэвис, П. (1994). Снижение концентрации переносчика глюкозы в головном мозге пациентов с болезнью Альцгеймера. Ann. Neurol. 36, 800–801. DOI: 10.1002 / ana.410360522
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Симс, Б., Пауэрс Р. Э., Сабина Р. Л. и Тайберт А. Б. (1998). Повышенная активность аденозинмонофосфатдезаминазы в мозге при болезни Альцгеймера. Neurobiol. Старение. 19, 385–391. DOI: 10.1016 / S0197-4580 (98) 00083-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Синке А. П., Джаякумар А. Р., Паникар К. С., Морияма М., Редди П. В. и Норенберг М. Д. (2008). NFkappaB в механизме индуцированного аммиаком набухания астроцитов в культуре. J. Neurochem. 106, 2302–2311. DOI: 10.1111 / j.1471-4159.2008.05549.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сонг Д. и Ду Т. (2014). Аммоний активирует сигнальный путь, активируемый уабаином, в астроцитах: терапевтический потенциал антагониста уабаина. Curr. Neuropharmacol. 12, 334–341. DOI: 10.2174 / 1570159X12666140828222115
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сперлинг, Р. А., Айзен, П. С., Беккет, Л.А., Беннетт, Д. А., Крафт, С., Фаган, А. М. и др. (2011). К определению доклинических стадий болезни Альцгеймера: рекомендации рабочих групп Национального института старения и ассоциации Альцгеймера по диагностическим руководствам по болезни Альцгеймера. Альцгеймера. Демент. 7, 280–292. DOI: 10.1016 / j.jalz.2011.03.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Вови, К. М., Ван, Ю., Уолш, П. Дж., И Перес-Пинзон, М. А. (2002). Сравнение эффектов аммиака на функцию митохондрий головного мозга крыс и морских обитателей. Am. J. Physiol. Regul. Интегр. Комп. Physiol. 283, R598 – R603. DOI: 10.1152 / ajpregu.00018.2002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Уорд А., Арриги Х. М., Михельс С. и Седарбаум Дж. М. (2012). Легкие когнитивные нарушения: несоответствие оценок заболеваемости и распространенности. Альцгеймера. Демент. 8, 14–21. DOI: 10.1016 / j.jalz.2011.01.002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Weihrauch, D., Зиглер А., Зиберс Д. и Тоул Д. В. (2002). Активная экскреция аммиака через жабры зеленого берегового краба Carcinus maenas: участие Na (+) / K (+) — АТФазы, H (+) — АТФазы V-типа и функциональных микротрубочек. J. Exp. Биол. 205 (Pt 18), 2765–2775.
PubMed Аннотация | Google Scholar
Вайнер И. Д. и Верландер Дж. У. (2003). Почечная и печеночная экспрессия белков-переносчиков аммония, гликопротеина Rh B и гликопротеина Rh C. Acta Physiol.Сканд. 179, 331–338. DOI: 10.1046 / j.0001-6772.2003.01210.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Райт, П. А. (1995). Выведение азота: три конечных продукта, многие физиологические роли. J. Exp. Биол. 198 (Pt 2), 273–281.
PubMed Аннотация | Google Scholar
Сюэ, З., Ли, Б., Гу, Л., Ху, X., Ли, М., Баттерворт, Р. Ф. и др. (2010). Повышенная экспрессия гена изоформы альфа2 Na, K-АТФазы аммиаком в астроцитах и головном мозге in vivo . Neurochem. Int. 57, 395–403. DOI: 10.1016 / j.neuint.2010.04.014
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Яо, Х., Ма, Э., Гу, X. К., и Хаддад, Г. Г. (1999). Регуляция внутриклеточного pH нейронов CA1 у мышей с мутантной изоформой 1 Na (+) / H (+). J. Clin. Вкладывать деньги. 104, 637–645. DOI: 10.1172 / JCI6785
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чжу, X., Перри, Г., Смит, М.А., и Ван, X. (2013). Аномальная митохондриальная динамика в патогенезе болезни Альцгеймера. J. Alzheimers. Дис. 33 (Дополнение 1), S253 – S262. DOI: 10.3233 / JAD-2012-129005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Zidi-Yahiaoui, N., Callebaut, I., Genetet, S., Le Van Kim, C., Cartron, J.P., Colin, Y., et al. (2009). Функциональный анализ человеческого RhCG: сравнение с транспортером аммония E. coli выявило сходство в порах и различия в преддверии. Am. J. Physiol. Cell Physiol. 297, C537 – C547. DOI: 10.1152 / ajpcell.00137.2009
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Зильке, Х. Р., Тилдон, Дж. Т., Зильке, К. Л., Бааб, П. Дж. И Ландри, М. Е. (1989). Функциональная внутриклеточная активность глутаминазы в интактных астроцитах. Neurochem. Res. 14, 327–332. DOI: 10.1007 / BF01000035
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Аммиак — обзор | Темы ScienceDirect
Сжигание смешанного топлива из метана и аммиака
Аммиак привлекает внимание как носитель водорода, имеющий большое содержание водорода, и ожидается, что он будет использоваться, в частности, в качестве топлива для выработки электроэнергии.На этот раз нам удалось создать газовую турбину, используя смесь газа из метана и аммиака, и продемонстрировать возможность выработки электроэнергии путем сжигания смеси аммиака на большой тепловой электростанции, использующей природный газ в качестве топлива. Кроме того, нам удалось выработать электроэнергию за счет 100% сжигания аммиака (специальное сжигание аммиака), что привело к крупномасштабному производству тепловой энергии без диоксида углерода (CO 2 ). Можно ожидать, что эти результаты будут применены на практике в качестве технологии, способствующей значительному сокращению выбросов парниковых газов в сфере производства электроэнергии.
Было продвинуто исследование и разработка носителей водорода, которые поддерживают массовое внедрение возобновляемых источников энергии, но аммиак имеет такие проблемы, как воспламенение менее легко, чем обычное топливо, и его скорость горения низкая. Производство энергии на газовых турбинах с использованием аммиака в качестве топлива до сих пор не производилось. Таким образом, производство энергии с помощью газовых турбин с использованием этого 100% аммиачного сырья является очень высоким достижением, а уровень технологий противодействия глобальному потеплению в Исследовательском центре возобновляемых источников энергии в Центре AIST в Фукусиме является выдающимся [87].
Обзор микрогазотурбинного электрогенератора, использованного для испытания на горение, показан на рис. 5.38.
Рисунок 5.38. Микрогазотурбинный генератор, который может сжигать аммиак напрямую.
Электрогенератор представляет собой газовую турбину номинальной мощностью 50 кВт. Нам удалось выработать 41,8 кВт при примерно 80% выходной мощности за счет совместного сжигания метана-аммиака и сжигания исключительно аммиака. Кроме того, был получен NOx, который представляет собой оксид азота после сгорания, который может быть снижен до уровня менее 10 ppm (рис.5.39).
Рисунок 5.39. Изменения в подаче топлива и выработке электроэнергии в эксперименте по сжиганию двухкомпонентного метана-аммиака.
Производство электроэнергии с использованием аммиака в качестве топлива было очень экологически чистым производством энергии, которое не выделяет углекислый газ, и оно показало чрезвычайно передовой результат, демонстрирующий возможность его практического использования.
В эксперименте по сжиганию монотоплива аммиака газовая турбина запускалась путем подачи керосина. После этого топливо было переведено на сжигание монотоплива аммиака за счет увеличения количества вводимого аммиака.
При подтверждении мощности в этот момент при номинальной скорости вращения 80 000 об / мин была подтверждена мощность выработки электроэнергии 41,8 кВт (рис. 5.40).
Рисунок 5.40. Изменения в подаче топлива и выработке электроэнергии в эксперименте по сжиганию монотоплива аммиака.
Эти экспериментальные результаты показывают, что возможно, что основное топливо для выработки тепловой энергии может быть переведено с природного газа на аммиак. Это предполагает, что аммиак может вводиться как часть топлива, или существует возможность сжигания только аммиака [88].
Это показывает возможность того, что аммиак может стать топливом для выработки электроэнергии, не содержащим CO 2 , что может значительно снизить выбросы парниковых газов.
Синтез аммиака непосредственно из воздуха и воды при температуре и давлении окружающей среды
Лан, Р., Ирвин, Дж. Т. С. и Тао, С. В. Аммиак и родственные ему химические вещества как потенциальные материалы для косвенного хранения водорода. Интер. J. Hydrogen Energy 37, 1482–1494 (2012).
CAS Статья Google Scholar
Бастидас, Д.М., Тао, С. В. и Ирвин, Дж. Т. С. Симметричный твердооксидный топливный элемент, демонстрирующий перовскитные электроды, устойчивые к окислительно-восстановительным процессам. J. Mater. Chem. 16, 1603–1605 (2006).
CAS Статья Google Scholar
Пул, Дж., Лобковский, Э. и Чирик, П. Гидрирование и расщепление диазота до аммиака с циркониевым комплексом. Nature 427, 527–530 (2004).
ADS CAS Статья Google Scholar
Амар, И.А., Лан, Р., Пети, К. Т. Г. и Тао, С. В. Твердотельный электрохимический синтез аммиака: обзор. J. Solid State Electrochem. 15. С. 1845–1860 (2011).
CAS Статья Google Scholar
http://www.kbr.com/Newsroom/Publications/Articles/Carbon-Dioxide-Capture-and-Storage-in-the-Nitrogen-Syngas-Industries.pdf. (Доступ 28 th августа 2012 г.).
http://www.decc.gov.uk/assets/decc/11/stats/climate-change/4282-statistical-release-2010-uk-greenhouse-gas-emissi.pdf. (Доступ 28 th августа 2012 г.).
Во, К. К., Батлер, Д. и Хайден, Б. Е. Механизм отравления катализаторов синтеза аммиака оксигенатами O2, CO и h3O — метод in situ для определения активной поверхности. Катал. Lett. 24. С. 197–210 (1994).
CAS Статья Google Scholar
Дженнингс Дж. Каталитический синтез аммиака: основы и практика. (Спрингер, 1991).
Chatt, J., Пирман, А. и Ричардс, Р. Восстановление монокоординированного молекулярного азота до аммиака в протонной среде. Nature 253, 39–40 (1975).
ADS CAS Статья Google Scholar
Яндулов Д. и Шрок Р. Каталитическое восстановление диазота до аммиака в одном молибденовом центре. Наука 301, 76 (2003).
ADS CAS Статья Google Scholar
Авенье, П.и другие. Диссоциация диазота на изолированном поверхностном атоме тантала. Наука 317, 1056 (2007).
ADS CAS Статья Google Scholar
Nishibayashi, Y. et al. Бакминстерфуллерены: неметаллическая система фиксации азота. Nature 428, 279–280 (2004).
ADS CAS Статья Google Scholar
Laplaza, C. & Cummins, C. Расщепление азота трехкоординированным комплексом молибдена (III).Наука 268, 861 (1995).
ADS CAS Статья Google Scholar
Химмель, Х. и Рейхер, М. Активация естественным азотом на атомах чистого металла. Энгью. Chem. Интер. Выпуск 45, 6264–6288 (2006).
CAS Статья Google Scholar
Шрок Р. Каталитическое восстановление диазота до аммиака молибденом: теория против эксперимента. Энгью.Chem. Интер. Выпуск 47, 5512–5522 (2008).
CAS Статья Google Scholar
Пикетт К. и Талармин Дж. Электросинтез аммиака. Nature 317, 652–653 (1985).
ADS CAS Статья Google Scholar
Фуруя Н. и Йошиба Х. Электровосстановление азота до аммиака на газодиффузионных электродах, модифицированных Fe-фталоцианином. Дж.Electroanalytical Chem. 263, 171–174 (1989).
CAS Статья Google Scholar
Фуруя Н. и Йошиба Х. Электровосстановление азота до аммиака на газодиффузионных электродах, модифицированных фталоцианинами металлов. J. Electroanalytical Chem. 272, 263–266 (1989).
CAS Статья Google Scholar
Норби Т. Твердотельные протонные проводники: принципы, свойства, развитие и перспективы.Ионика твердого тела 125, 1–11 (1999).
CAS Статья Google Scholar
Кройер, К. Д. Протонная проводимость: материалы и применения. Chem. Матер. 8, 610–641 (1996).
CAS Статья Google Scholar
Ивахара, Х., Эсака, Т., Учида, Х. и Маеда, Н. Протонная проводимость в спеченных оксидах и ее применение в паровом электролизе для производства водорода.Ионика твердого тела 3–4, 359–363 (1981).
Артикул Google Scholar
Тао, С. В. и Ирвин, Дж. Т. С. Стабильный, легко спекаемый протонпроводящий оксидный электролит для топливных элементов и электролизеров при умеренных температурах. Adv. Матер. 18, 1581–1584 (2006).
CAS Статья Google Scholar
Марнеллос Г. и Стоукидес М. Синтез аммиака при атмосферном давлении.Science 282, 98–100 (1998).
ADS CAS Статья Google Scholar
Skodra, A. & Stoukides, M. Электрокаталитический синтез аммиака из пара и азота при атмосферном давлении. Ионика твердого тела 180, 1332–1336 (2009).
CAS Статья Google Scholar
Мураками Т., Нохира Т., Гото Т., Огата Ю. Х. и Ито Ю. Электролитический синтез аммиака из воды и газообразного азота в расплаве соли при атмосферном давлении.Электрохим. Acta 50, 5423–5426 (2005).
CAS Статья Google Scholar
Murakami, T. et al. Электролитический синтез аммиака из воды и азота при атмосферном давлении с использованием алмазного электрода, легированного бором, в качестве неплавящегося анода. Электрохим. & Solid State Lett. 10, E4 – E6 (2007).
CAS Статья Google Scholar
Амар, И.А., Лан, Р., Пети, К. Т. Г., Арриги, В. и Тао, С. В. Электрохимический синтез аммиака на основе карбонатно-оксидного композитного электролита. Ионика твердого тела 182 (2011), 133–138.
CAS Статья Google Scholar
Перман, Э. и Аткинсон, Г. Разложение аммиака при нагревании. Труды Лондонского королевского общества 74, 110–117 (1904).
ADS Статья Google Scholar
Кунду, П.П. и Пал, А. Катионообменные полимерные мембраны для топливных элементов. Обзоры в химической инженерии 22, 125–153 (2006).
CAS Статья Google Scholar
Кордали В., Кириаку Г. и Ламброу К. Электрохимический синтез аммиака при атмосферном давлении и низкой температуре в ячейке с твердым полимерным электролитом. Chem. Comm. 1673–1674 (2000).
Чжан, З. Ф., Чжун, З. П., Лю Р. К. Катодные характеристики катодного катализа SmBaCuMO5 + δ (M = Fe, Co, Ni) в синтезе аммиака.J. Rare Earths 28, 556–559 (2010).
CAS Статья Google Scholar
Skulason, E. et al. Теоретическая оценка возможных электрокатализаторов на основе переходных металлов для восстановления N2. Phys. Chem. Chem. Phys. 14. С. 1235–1245 (2012).
CAS Статья Google Scholar
Бернс Р. и Харди Р. Фиксация азота у бактерий и высших растений. Молекулярная биология, биохимия и биофизика 21, 1–189 (1975).
Google Scholar
Benemann, J. & Valentine, R. Пути фиксации азота. Успехи микробной физиологии 8, 59–104 (1972).
CAS Статья Google Scholar
Хунсирикарн К., Гудвин Дж. Мл., Гринуэй С. и Крегер С. Влияние аммиака на проводимость мембран Nafion. J. Источники энергии 195, 30–38 (2010).
ADS CAS Статья Google Scholar
Москвич, Ю.Н., Поляков А.М., Суховский А.А. ЯМР-исследование ионных движений и механизмов проводимости в протонных проводниках MHSeO4 и M3H (AO4) 2. Сегнетоэлектрики, 81, 1161–1164 (1988).
Артикул Google Scholar
Pawowski, A., Pawlaczyk, C. & Hilczer, B. Электропроводность в кристаллической группе Me3H (SeO4) 2 (Me: NH 4+ , Rb + , Cs + ). Ионика твердого тела 44, 17–19 (1990).
Артикул Google Scholar
Бинньюис, М.& Milke, E. Термохимические данные элементов и соединений. (Интернет-библиотека Wiley, 1999).
Янг, С. К., Тревино, С. и Бек Тан, Н. С. Исследование структурных изменений мембран нафиона, вызванных набуханием различными растворителями, с помощью малоуглового рассеяния нейтронов. Journal of Polymer Science Part B: Polymer Physics 40, 387–400 (2002).
ADS CAS Статья Google Scholar
Halseid, R., Ви, П. Дж. С. и Тунольд, Р. Влияние аммиака на характеристики топливных элементов с полимерным электролитом с мембраной. J. Источники энергии 154, 343–350 (2006).
ADS CAS Статья Google Scholar
Харгривз, Дж. С. Дж. И Маккей, Д. Сравнение реакционной способности решеточного азота в катализаторах Co3Mo3N и Ni2Mo3N. J. Mol. Катал. A-Chem. 305. С. 125–129 (2009).
CAS Статья Google Scholar
10 разумных способов использования аммиака
Фото: istockphoto.com
Аммиак — это просто потрясающе! Как газ, это химическое соединение водорода и азота едкое и опасное. Но разбавленная бытовая форма, суперочиститель на основе азота, незаменима в борьбе с обычной бытовой грязью и сажей. Он настолько универсален, что с ним можно справиться с множеством дел — от достижения блеска без разводов на стекле до исчезновения даже самых жирных пятен. Его легко найти где угодно, от местного продуктового магазина до торговых площадок электронной коммерции, таких как Amazon. Бутылка на 64 унции обычно стоит менее 5 долларов, и это тоже крепкая вещь, так что небольшая часть имеет большое значение.Этот недорогой кувшин, который вы покупаете сегодня, должен намного пережить более современные коммерческие чистящие средства.
Перед тем, как отправиться за покупками, знайте, что есть различные типы бытового аммиака на выбор. Вы можете увидеть «мутные» или «пенные» варианты — это аммиак с добавлением мыла, который обычно используется для такой домашней уборки, как обработка запачканной одежды или мытье кухонных плит. Но «чистый» аммиак подходит для более широкого круга задач (и вы всегда можете добавить столовую ложку или две средства для мытья посуды, чтобы получить прозрачную мыльную пену с аммиаком).Вы также найдете аммиак с запахом лимона или сосны, чтобы смягчить резкий запах.
Однако резкий запах служит предупреждением: работа с аммиаком абсолютно требует осторожности. Чистый химический аммиак может вызвать серьезные ожоги и проблемы с дыханием при контакте с кожей или проглатывании. Даже разбавленный водой, как это рекомендуется для большинства целей очистки, аммиак все равно может быть вредным.
СВЯЗАННЫЕ С: 11 опасностей в ванной комнате, которые вредят вашему дому и здоровью
Самое важное правило безопасности, которое следует помнить: никогда не смешивайте аммиак с хлорным отбеливателем.В результате получается высокотоксичный газообразный хлор, который может вызывать головные боли, судороги и другие симптомы. Очень важно помнить об этом при использовании нашатырного спирта для стирки или для чистки поверхностей, не смешивая его с моющим средством или бытовым чистящим средством, содержащим отбеливатель.
Всегда надевайте химически стойкие перчатки и хорошо проветривайте помещение при использовании аммиака. И обязательно храните его в недоступном для домашних животных и детей месте. Соблюдайте эти меры предосторожности, применяя аммиак для выполнения 10 задач здесь — и наслаждайтесь безупречным домом за копейки!
1.Conquer Conquer StainsОбесцвечивание бетонной подъездной дороги, пола гаража или патио может вызвать раздражение. Смешайте 1 стакан нашатырного спирта с 1 галлоном воды в ведре и нанесите его на пятна с помощью большой губки или швабры. Оставьте на 20 минут, а затем потрите пятно щеткой с щетиной. Промойте это место чистой водой или промойте его из шланга. Если пятно не исчезло полностью после того, как область высохла, повторяйте процесс, пока не будете удовлетворены результатами.
2. Стекло для сияния блескаЧтобы добиться на зеркалах, окнах и кристаллах без полос, смешайте 1 столовую ложку чистого нашатырного спирта с 2 стаканами воды в пульверизаторе.Распылите раствор на стеклянные предметы и немедленно вытрите насухо мягкой безворсовой тканью для окон и хрусталя; бумажные полотенца отлично подходят для зеркал.
Фото: istockphoto.com
3. Предварительная обработка пятен от бельяУстойчивые пятна на хлопчатобумажных, полиэфирных или нейлоновых тканях не подходят для раствора из стакана чистого аммиака, ⅔ стакана средства для мытья посуды, 6 столовых ложек пищевой соды. и 2 стакана теплой воды. Смешайте в миске или ведре и обильно нанесите губкой или пульверизатором.Оставьте на 30 минут и постирайте как обычно. Если он окажется слишком разбавленным для более сильных пятен, таких как кровь или трава, снова обработайте его раствором, состоящим из одной части нашатырного спирта и одной части теплой воды.
Примечание. Не используйте этот метод для шерсти или шелка; аммиак может разъесть эти нежные ткани. И помните, что никогда не смешивайте нашатырный спирт с любыми средствами для стирки, содержащими отбеливатель.
4. Избавьтесь от смазки на горелкахС помощью этой уловки избавьтесь от очень вязкой смазки на горелках.Поместите каждую горелку в отдельный герметичный пластиковый пакет, наполненный стакана аммиака. Закройте каждый пакет, чтобы не допустить испарений, и поместите в раковину или таз на 8–12 часов. Откройте пакеты в проветриваемом помещении и легко удалите весь жир и грязь с помощью средства для мытья посуды и воды. Как только грязь исчезнет, тщательно промойте горелки водой, чтобы избавиться от остатков аммиака. Дайте полностью высохнуть перед использованием.
5. Очистите пятна ковра и обивкиСмешайте одну часть чистого аммиака и одну часть горячей воды в распылителе или другой бутылке.Обильно нанесите на пятно спринтом или губкой. Примерно через 10 минут наложите на пятно чистое старое полотенце и прижмите утюгом, продувая паром, примерно на 20 секунд. Проверьте свой прогресс: пятно должно начать переходить на полотенце. Повторите эти действия с глажением с паром и добавлением раствора нашатыря, если необходимо, пока пятно не исчезнет.
6. Электрическая духовка Sparkle UpНагрейте духовку до 150 градусов, пока кипятите большую кастрюлю с водой на плите.Выключите духовку и откройте окна, чтобы проветрить кухню. Поставьте прочную емкость, например стеклянный мерный стакан или металлическую миску, наполненную ½ стакана нашатырного спирта на верхнюю полку духовки, а кастрюлю с кипяченой водой — на нижнюю. Закройте духовку и оставьте на 8-12 часов, затем удалите нашатырный спирт и воду. Держите дверцу духовки открытой и дайте ей проветриться не менее часа, прежде чем приступить к уборке. Поскольку грязь погрязла в парах аммиака, ее следует разрыхлить и легко удалить губкой, теплой водой и мылом для посуды.
Этот метод рекомендуется только для электрических духовок, так как смешивание аммиака с газом может быть опасным. Если вы хотите использовать этот метод на своей газовой духовке, убедитесь, что контрольная лампа и газовые линии выключены.
Фото: istockphoto.com
7. Обновить плиткуПлитка для кухни или ванной выглядит уставшей? Чтобы очистить и продезинфицировать их, смешайте ¼ стакана аммиака с 1 галлоном воды в ведре и обильно нанесите раствор губкой или шваброй. Если участок особенно грязный, используйте щетку с мягкой щетиной, чтобы соскрести грязь.В конце протрите всю поверхность чистой водой и губкой или шваброй.
8. Сделайте сияние ярче!Если золотые, серебряные, бриллиантовые или платиновые украшения потеряли свой блеск, смешайте шесть частей теплой воды с одной частью нашатырного спирта в миске или небольшом ведре, в котором вы не едите и не готовите, и добавьте свои драгоценные кусочки. Через 15 минут снимите украшение рукой в перчатке, а затем аккуратно соскребите стойкую грязь зубной щеткой с мягкой щетиной (той, которая больше не используется или предназначена для чистки).Дайте ему впитаться еще 15 минут, удалите из раствора и немедленно смойте теплой водой. (Слейте использованный раствор нашатырного спирта в канализацию, пропуская горячую воду.) Затем отполируйте украшения мягкой тканью без ворса и дайте им высохнуть.
Не используйте этот метод для жемчуга, так как аммиак может разрушить нежную отделку или другие драгоценные камни, поскольку многие камни теперь проходят масляную обработку, которую можно удалить аммиаком.
9. Send Smells PackingАммиак устойчив к любому запаху от свежей краски до горелой лазаньи.Поместите небольшую емкость, наполненную примерно половиной стакана чистого аммиака, рядом с неприятным запахом, следя за тем, чтобы проветривать помещение, чтобы он поглотил неприятный запах в течение нескольких часов.
10. Держите вредителей в бухтеСильный запах аммиака может отпугнуть нежелательных животных. Наполните блюдце чистым нашатырным спиртом без запаха или пропитайте им тряпку или ватные шарики. Затем разместите в местах, привлекающих вредителей, например, возле мусорных баков, где крадутся еноты, или рядом с трещинами в подвале, куда заходят мыши.Запах напомнит варминтам о хищниках, поэтому они, скорее всего, уловят запах и отвернутся, невредимые. Тем не менее, убедитесь, что средство отпугивания аммиака находится в недоступном для детей и домашних животных месте.
Экологические эффекты аммиака | Департамент сельского хозяйства Миннесоты
Даже при очень низких концентрациях аммиак будет вреден для водных организмов. Аммиак естественным образом встречается в окружающей среде. Небольшое количество аммиака образуется при ударе молнии и достигает земли во время дождя. Но большая часть аммиака производится бактериями в воде и почве как конечный продукт разложения растительных и животных отходов.Он содержится в относительно низких нетоксичных концентрациях в почве, воздухе и воде и является источником азота для растений.В почвах и воде аммиак претерпит множество сложных биохимических преобразований. Эти превращения составляют так называемый азотный цикл. Для более подробного обсуждения азотного цикла см. Связанные ссылки.
Аммиак в воде
Вода реагирует с аммиаком с образованием ионов аммония и гидроксида. Аммиак часто называют «неионизированным аммиаком».Аммиак токсичен для водных организмов, но аммоний нетоксичен. В воде существует равновесие между токсичным аммиаком и нетоксичным аммонием. Уравнение смещается вперед и назад в зависимости от существующих или внесенных изменений окружающей среды
На динамическое равновесие между Nh4 и Nh5 + влияют температура воды и pH (кислотность). При pH, равном шести, отношение аммиака к аммонию составляет от 1 до 3000, но уменьшается до 1–30, когда pH повышается до восьми (становится менее кислым).Теплая вода будет содержать больше токсичного аммиака, чем холодная вода. При отборе проб воды для анализа аммиака температура и pH поверхностного водного объекта должны измеряться одновременно с отбором проб воды. (См. Калькулятор аммиака, pH и температуры)
Если аммиак проливается непосредственно в поверхностные воды или если вода, используемая пожарной частью для подавления облака паров аммиака, достигает поверхностных вод, это может причинить вред водным организмам. Даже при концентрации 0.Неионизированный аммиак в концентрации 02 мг / л (48 часов LC50) является смертельным для некоторых чувствительных пресноводных рыб. Это равняется примерно ½ стакана неионизированного аммиака на один миллион галлонов воды. Аммиак также очень токсичен для пресноводных беспозвоночных, так как ЛК50 за 48 часов для Daphnia magna составляет 0,66 мг / л. Опять же, вода, загрязненная аммиаком для удобрений, не должна попадать в ливневые стоки, реки, дренажные канавы, водно-болотные угодья или озера.
Аммиак в воздухе и почве
После выброса аммиака пары рассеиваются, вступая в реакцию с влагой в воздухе, с образованием аммония и в конечном итоге возвращаются на землю в виде дождя.Затем аммоний быстро связывается с отрицательно заряженными органическими веществами почвы и почвенными глинами. Аммоний редко накапливается в почве, потому что бактерии быстро превращают аммоний, который не усваивается корнями растений, в нитраты (нитрификация). Нитраты также могут абсорбироваться корнями или вымываться через профиль почвы. Поскольку аммоний связан с почвой, если почва не смывается дождями, загрязнение, скорее всего, останется горизонтальным, но выщелачивается вертикально в виде нитратов через корневую зону.
Если пожарная часть подавляет облако паров аммиака водой в течение длительного периода времени, применяемая вода может загрязнить почву. В этом случае почве может потребоваться какой-либо метод восстановления, чтобы предотвратить неблагоприятное воздействие на окружающую среду.
Растения, поражающие аммиаком
Растения, деревья и зерновые культуры в основном состоят из воды. Если произойдет большой выброс аммиака, пар, скорее всего, сожжет листья близлежащей растительности с подветренной стороны. Аммиак вытягивает воду из листьев, но не влияет на корни, поэтому поврежденные растения, вероятно, полностью восстановятся, хотя пораженные культуры могут потерять урожай.
Аммиак, влияющий на домашний скот
Имейте в виду, что пары аммиака токсичны для домашнего скота. Производители молочного, свиного и птицеводческого животноводства, работающие вблизи и с подветренной стороны от выброса или потенциального выброса, должны быть уведомлены о принятии соответствующих мер.
Цикл азота в почве из информационного бюллетеня по расширению Университета штата Огайо AEX-463-96
% PDF-1.5 % 4 0 obj > эндобдж xref 4 89 0000000016 00000 н. 0000002374 00000 н. 0000002470 00000 н. 0000003127 00000 н. 0000003407 00000 н. 0000003807 00000 н. 0000004309 00000 н. 0000004484 00000 н. 0000004922 00000 н. 0000005240 00000 п. 0000005275 00000 н. 0000005320 00000 н. 0000012383 00000 п. 0000018943 00000 п. 0000019078 00000 п. 0000025966 00000 п. 0000032268 00000 п. 0000039220 00000 п. 0000046101 00000 п. 0000046484 00000 п. 0000052860 00000 п. 0000060353 00000 п. 0000063001 00000 п. 0000063600 00000 п. 0000063713 00000 п. 0000063826 00000 п. 0000063941 00000 п. 0000064052 00000 п. 0000064121 00000 п. 0000064213 00000 п. 0000072273 00000 п. 0000072546 00000 п. 0000072814 00000 п. 0000072839 00000 п. 0000073231 00000 п. 0000074221 00000 п. 0000074498 00000 п. 0000074828 00000 п. 0000076899 00000 н. 0000077220 00000 п. 0000077612 00000 п. 0000077695 00000 п. 0000082381 00000 п. 0000082826 00000 п. 0000083359 00000 п. 0000083466 00000 п. 0000083992 00000 п. 0000084292 00000 п. 0000084605 00000 п. 0000086644 00000 п. 0000086948 00000 п. U_cyY.{&; apOf1 (FC VBK01 ~ efT` (Θ {5) = ‘x002j (] Hr3g4dŘ`Gy67suiF `
Воздействие выбросов аммиака и сероводорода от животноводства
Выбросы аммиака влияют на здоровье человека и экосистемы, в то время как сероводород в первую очередь является проблемой для здоровья человека.
Выбросы в атмосферу от предприятий по производству кормов для животных, больших и малых, коммерческих и любительских ферм невозможно полностью избежать. Усилия по сокращению этих выбросов могут улучшить здоровье экосистемы, здоровье человека и отношения с соседями.Важно понимать, какое влияние оказывают выбросы в атмосферу. Здесь рассматриваются два наиболее известных выброса — аммиак и сероводород.
Аммиак (NH 3 ) — это газ, образующийся в результате неполного преобразования исходного азота в продукты животного происхождения (мясо и / или молоко). Хотя домашний скот, выращиваемый на коммерческих фермах, более эффективно использует питательные вещества корма, чем большинство людей, не все питательные вещества в корме превращаются в продукт (рост, мясо, молоко, яйца, потомство).Аль Ротц 3 газ. Атмосферный NH 3 является важным загрязнителем из-за его воздействия на экосистемы. Слишком большое количество NH 3 в воздухе может привести к осаждению в поверхностные воды в результате дождя и вызвать чрезмерное обогащение или эвтрофикацию поверхностных вод (цветение водорослей). Осаждение часто происходит далеко от места добычи газа NH 3 . Вспышки красных приливов в Чесапикском заливе частично объясняются чрезмерным обогащением азотом. сообщили в 2004 году, что эффективность преобразования азота в животноводстве может варьироваться от 20 до 40 процентов.Таким образом, значительное количество азота, содержащегося в кормах для животных, выводится с мочой и фекалиями и может преобразовываться в NH
.Газообразный аммиак может реагировать в атмосфере с другими газообразными соединениями (кислотами, например, кислотами, возникающими в результате природных процессов на суше или при добыче угля) с образованием мелкодисперсных частиц (аэрозолей аммония (NH 4 + )), которые имеют следующие свойства: проблема со здоровьем. Эти мелкодисперсные частицы (называемые PM 2,5 3 и NH 4 + ) задерживаются в атмосфере в течение нескольких дней и могут переноситься на сотни миль; при рассмотрении воздействия NH на окружающую среду необходима перспектива регионального масштаба. 3 .частицы) являются раздражителями дыхательных путей. Поскольку и аммиак, и аммоний (NH
Хотя здесь основное внимание уделяется внутрихозяйственным источникам выбросов, концентрации NH 3 в наших собственных домах могут быть такими же высокими, как и на сельскохозяйственных территориях, особенно когда присутствуют концентрированные чистящие средства, туалетные лотки и даже курильщики.
Сероводород (H 2 S) наиболее известен своим характерным запахом: тухлыми яйцами. При высоких концентрациях сероводород может быть смертельно опасным (силосный газ).H 2 S даже в низких концентрациях вызывает раздражение дыхательных путей. Хотя сероводород не переносится на большие расстояния, на ферме он может смешиваться с другими соединениями, создавая запах. По сравнению с NH 3 , выбросы H 2 S довольно низкие; часто они в 10 и более раз ниже, чем выбросы NH 3 . H 2 S образуется в анаэробных условиях (отсутствие кислорода), поэтому источники H 2 S в основном происходят из хранилищ навоза, тогда как NH 3 2 S выделяется как из помещений для животных, так и из хранилищ навоза.В некоторых штатах есть стандарты линии собственности H 2 S (Айова и Миннесота). Проблемы, соответствующие государственному стандарту, возникли в результате размещения открытых хранилищ навоза рядом с границей участка и / или ненадлежащей практики управления фермерским хозяйством.
Вы нашли эту статью полезной?
Расскажите, пожалуйста, почему
Представлять на рассмотрение .
 Для этого осторожно подносят небольшой кусок ваты или марли, смоченной нашатырным спиртом к носовым отверстиям (буквально на мгновение) или применяют ампулу с оплеткой: при отламывании кончика ампулы ватно-марлевая оплетка пропитывается раствором. Известны и нашатырно-анисовые капли как отхаркивающее средство, например, при бронхитах. Иногда нашатырный спирт применяют внутрь в качестве рвотного средства, но только в разведенном виде (5-10 капель на 100 мл воды). При укусах насекомых применяют наружно в виде примочек. Специалистам известно, что раствор аммиака применяют в хирургической практике для мытья рук.
Для этого осторожно подносят небольшой кусок ваты или марли, смоченной нашатырным спиртом к носовым отверстиям (буквально на мгновение) или применяют ампулу с оплеткой: при отламывании кончика ампулы ватно-марлевая оплетка пропитывается раствором. Известны и нашатырно-анисовые капли как отхаркивающее средство, например, при бронхитах. Иногда нашатырный спирт применяют внутрь в качестве рвотного средства, но только в разведенном виде (5-10 капель на 100 мл воды). При укусах насекомых применяют наружно в виде примочек. Специалистам известно, что раствор аммиака применяют в хирургической практике для мытья рук. Кроме того, аммиак – горючий газ, а высокие концентрации его в воздухе взрывоопасны.
Кроме того, аммиак – горючий газ, а высокие концентрации его в воздухе взрывоопасны. В результате выброса 40 т аммиака 15 человек получили отравление. В Москве произошел выброс аммиака на Бирюлевском мясоперерабатывающем комбинате в результате пробоя трубопровода подачи аммиака, 20 человек были эвакуированы.
В результате выброса 40 т аммиака 15 человек получили отравление. В Москве произошел выброс аммиака на Бирюлевском мясоперерабатывающем комбинате в результате пробоя трубопровода подачи аммиака, 20 человек были эвакуированы. Слизистые и глаза следует промывать не менее 15 минут водой или 2% раствором борной кислоты. В глаза закапывают 2-3 капли 30% раствора альбуцида в нос – теплое оливковое, персиковое или вазелиновое масло. Пораженную кожу необходимо облить чистой водой, наложить примочки из 5% раствора уксусной, лимонной или соляной кислоты.
Слизистые и глаза следует промывать не менее 15 минут водой или 2% раствором борной кислоты. В глаза закапывают 2-3 капли 30% раствора альбуцида в нос – теплое оливковое, персиковое или вазелиновое масло. Пораженную кожу необходимо облить чистой водой, наложить примочки из 5% раствора уксусной, лимонной или соляной кислоты.